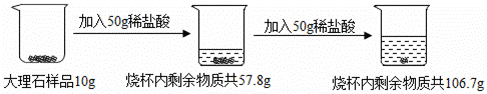
(2020·巴中模拟)向10g大理石样品中分两次加入一定溶质质量分数的稀盐酸(杂质不溶于水,也不与稀盐酸反应),充分反应后烧杯内物质总质量的变化如图所示。
请计算:
(1)生成二氧化碳的质量为________g。
(2)所用稀盐酸的溶质质量分数。(写出计算过程)
(1)稀盐酸和碳酸钙反应生成氯化钙和水、二氧化碳,根据质量守恒定律可得,生成的二氧化碳的总质量为10g+50g+50g-106.7g=3.3g
(2)由于加入第一个50g稀盐酸对应生成10g+50g-57.8g=2.2g二氧化碳,所以生成3.3g二氧化碳时消耗的盐酸的质量为75g,即第二次加入的稀盐酸剩余,设所用稀盐酸的溶质质量分数为 x,
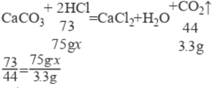
![]()
解得 x=7.3%
答:所用稀盐酸的溶质质量分数为7.3%
【解析】解:(1)稀盐酸和碳酸钙反应生成氯化钙和水、二氧化碳,根据质量守恒定律可得,生成的二氧化碳的总质量为10g+50g+50g-106.7g=3.3g。
(2)由于加入第一个50g稀盐酸对应生成10g+50g-57.8g=2.2g二氧化碳,所以生成3.3g二氧化碳时消耗的盐酸的质量为75g,即第二次加入的稀盐酸剩余,设所用稀盐酸的溶质质量分数为 x,

解得 x=7.3%
答:所用稀盐酸的溶质质量分数为7.3%。
【分析】(1)根据质量守恒定律可得,生成的二氧化碳的总质量=反应物质总质量-反应后烧杯里剩余的质量。
(2)根据反应图,第一次加入50g盐酸,盐酸恰好完全反应,计算出生成二氧化碳的质量。再根据化学方程式进行计算。
(2020·金堂模拟)实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验的相关数据如图。
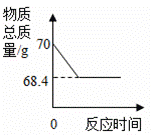
(1)二氧化锰作为催化剂在化学反应前后本身的________和________都没有发生变化。
(2)过氧化氢中氧元素的化合价为________;反应生成氧气的质量为________g。
(3)参加反应的过氧化氢溶液中溶质质量分数是多少?(写出计算过程)
(1)质量;化学性质
(2)-1;1.6
(3)解:设过氧化氢质量为y。

参加反应的过氧化氢溶液中溶质质量分数= ![]() 。
。
答:参加反应的过氧化氢溶液中溶质质量分数5%。
【解析】(1)催化剂能改变其他物质的反应速率,反应前后本身的质量和化学性质都不变的物质,二氧化锰作为催化剂在化学反应前后本身的质量和化学性质都没有发生变化;
(2)根据化合价代数和为零,设:氧元素化合价为x , 则有:(+1)×2+x×2=0,故x=-1;根据质量守恒反应生成氧气质量70g-68.4g=1.6g;
【分析】(1)根据催化剂的特点进行分析。
(2)根据在化合物中,元素的正负化合价代数和为零,进行计算。
根据质量守恒定律可知,反应前后物质的总质量不变,进行计算出生成氧气的质量。
(3)先设未知数,正确写出过氧化氢制取的化学方程式;再找准有关物质,已知量是氧气的质量,未知量是过氧化氢的质量;列比例式计算。
(2020·顺庆模拟)如图为某牙膏的部分标签,活性成分单氟磷酸钠的化学式为Na2PO3F(相对分子质量为 144),请回答下列问题:

(1)人体中 F 属于________(填“微量”或“常量”)元素。
(2)若牙膏中其它成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为多少g(结果保留整数)。
(1)微量
(2)2.1
【解析】(1)在人体内含量大于0.01%的是常量元素,否则属于微量元素,人体内的常量元素主要有:氧、碳、氢、氮、钙、磷、钾、硫、钠、氯、镁;微量元素主要有:铁、钴、铜、锌、铬、锰、钼、氟、碘、硒。F属于微量元素。(2)每支这种牙膏中氟元素的质量为200g×0.14%=0.28g。设含Na2PO3F的质量为x , 则 ![]() ;x≈2.1g;
;x≈2.1g;
答:含 Na2PO3F的质量为2.1g
【分析】(1)根据人体的微量元素和常量元素分析
(2)根据元素质量等于物质质量乘以元素的质量分数分析
(2020·高新模拟)我国是世界钢铁产量最大的国家,炼铁的主要原料是铁矿石。用赤铁矿石(主要成分为Fe2O3)炼铁的反应原理为:Fe2O3+3CO ![]() 2Fe+3CO2。
2Fe+3CO2。
(1)上述反应不是置换反应的理由是:________。
(2)根据化学式计算:Fe2O3中铁元素的质量分数________。
(3)根据化学方程式计算:用含Fe2O360%的赤铁矿石800t,理论上可炼出纯铁多少吨________?
(1)置换反应反应物是单质和化合物,生成物也必须是单质和化合物上述反应反应物都是化合物不符合要求,不属于置换反应。
(2)70%
(3)336吨
【解析】(1)根据置换反应的定义单质和化合物生成单质和化合物的化学反应属于置换反应炼铁反应物都是化合物不属于置换反应;(2)Fe2O3中铁元素的质量分数 ![]() ,故填:70%;(3)设理论上可炼出铁的质量为x
,故填:70%;(3)设理论上可炼出铁的质量为x
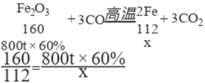
x=336t
答:理论上可炼出纯铁336吨。
【分析】本题考察化学方程式的一般应用,通过化学方程式来计算反应物或生成物质量,计算的时候需要注意纯量的代入,混合物要转化为纯净物质量,溶液质量要转化为溶质质量。
(2020·广东模拟)
(1)(一)某校化学兴趣小组同学用以下装置对质量守恒定律进行实验探究。
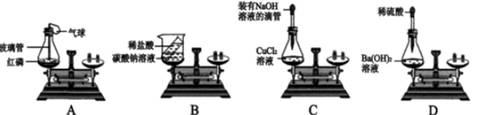
实验A的化学方程式为________,实验完毕天平保持平衡的是________(填序号)。
(2)(二)实验完毕,兴趣小组的同学将B、C实验的废液(含C中的蓝色沉淀)混合,得到蓝色沉淀及无色溶液。过滤,并对无色滤液的成分进行以下实验分析:
【做出猜想】猜想I:只含NaCl; 猜想II:含有NaCl、________; 猜想III:含有NaCl与NaOH;
猜想IV:含有NaCl、NaOH与Na2CO3。
(3)【进行实验】
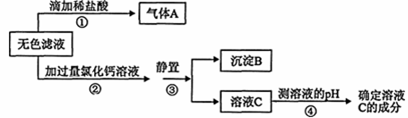
a.步骤④的操作是:在玻璃片上放一小片pH试纸,然后________,读出pH值。
b.步骤②的化学方程式为________。
c.根据步骤①,可确定无色滤液的溶质除了NaCl外还含有________,如果步骤④的结果是溶液pH=11,则溶液C除了NaCl外含有的溶质是________,结合步骤①可确定猜想________成立。
(1)4P+5O2 ![]() 2P2O5;ACD
2P2O5;ACD
(2)Na2CO3
(3)用玻璃棒沾取待测液滴到pH试纸上,与标准比色卡比较;Na2CO3+CaCl2=CaCO3↓+2NaCl;Na2CO3;NaOH;IV
【解析】(1)A中磷和氧气点燃生成五氧化二磷,方程式为 4P+5O2 ![]() 2P2O5 ,B中碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,C中氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,氢氧化钡和稀硫酸反应生成硫酸钡和水,因此天平保持平衡的是ACD;
2P2O5 ,B中碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,C中氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,氢氧化钡和稀硫酸反应生成硫酸钡和水,因此天平保持平衡的是ACD;
(2) 将B、C实验的废液(含C中的蓝色沉淀)混合,得到蓝色沉淀及无色溶液,说明C中剩余氯化铜,B中剩余碳酸钠,氯化铜和碳酸钠反应生成碳酸铜和氯化钠,因此反应后的滤液中可能含有碳酸钠和氯化钠
(3)测定溶液pH时, 用玻璃棒沾取待测液滴到pH试纸上 , 然后与标准比色卡比较
步骤② 是碳酸钠和氯化钙反应生成碳酸钙和氯化钠,方程式为 Na2CO3+CaCl2=CaCO3↓+2NaCl
由于产生了白色沉淀,因此根据步骤①,可确定无色滤液的溶质除了NaCl外还含有碳酸钠, 如果步骤④的结果是溶液pH=11,则溶液C除了NaCl外含有的溶质是 氢氧化钠, 结合步骤①可确定猜想 IV 成立;
【分析】(1)根据林和氧气点燃生成五氧化二磷及各装置中发生的反应分析
(2)根据两支试管中含有的物质及发生的反应分析
(3)根据测定溶液pH的方法是碳酸钠和和氯化钙反应生成碳酸钙和氯化钠分析
本卷还有45题,登录并加入会员即可免费使用哦~

该作品由: 用户ZZ47分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。