(2020·高新模拟)我国是世界钢铁产量最大的国家,炼铁的主要原料是铁矿石。用赤铁矿石(主要成分为Fe2O3)炼铁的反应原理为:Fe2O3+3CO ![]() 2Fe+3CO2。
2Fe+3CO2。
(1)上述反应不是置换反应的理由是:________。
(2)根据化学式计算:Fe2O3中铁元素的质量分数________。
(3)根据化学方程式计算:用含Fe2O360%的赤铁矿石800t,理论上可炼出纯铁多少吨________?
答案
(1)置换反应反应物是单质和化合物,生成物也必须是单质和化合物上述反应反应物都是化合物不符合要求,不属于置换反应。
(2)70%
(3)336吨
【解析】(1)根据置换反应的定义单质和化合物生成单质和化合物的化学反应属于置换反应炼铁反应物都是化合物不属于置换反应;(2)Fe2O3中铁元素的质量分数 ![]() ,故填:70%;(3)设理论上可炼出铁的质量为x
,故填:70%;(3)设理论上可炼出铁的质量为x
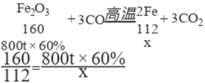
x=336t
答:理论上可炼出纯铁336吨。
【分析】本题考察化学方程式的一般应用,通过化学方程式来计算反应物或生成物质量,计算的时候需要注意纯量的代入,混合物要转化为纯净物质量,溶液质量要转化为溶质质量。

