(2020·广东模拟)
(1)(一)某校化学兴趣小组同学用以下装置对质量守恒定律进行实验探究。
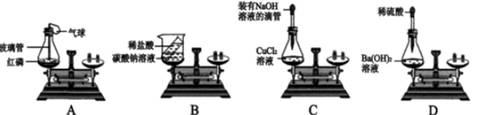
实验A的化学方程式为________,实验完毕天平保持平衡的是________(填序号)。
(2)(二)实验完毕,兴趣小组的同学将B、C实验的废液(含C中的蓝色沉淀)混合,得到蓝色沉淀及无色溶液。过滤,并对无色滤液的成分进行以下实验分析:
【做出猜想】猜想I:只含NaCl; 猜想II:含有NaCl、________; 猜想III:含有NaCl与NaOH;
猜想IV:含有NaCl、NaOH与Na2CO3。
(3)【进行实验】
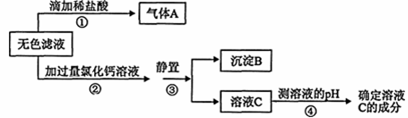
a.步骤④的操作是:在玻璃片上放一小片pH试纸,然后________,读出pH值。
b.步骤②的化学方程式为________。
c.根据步骤①,可确定无色滤液的溶质除了NaCl外还含有________,如果步骤④的结果是溶液pH=11,则溶液C除了NaCl外含有的溶质是________,结合步骤①可确定猜想________成立。
答案
(1)4P+5O2 ![]() 2P2O5;ACD
2P2O5;ACD
(2)Na2CO3
(3)用玻璃棒沾取待测液滴到pH试纸上,与标准比色卡比较;Na2CO3+CaCl2=CaCO3↓+2NaCl;Na2CO3;NaOH;IV
【解析】(1)A中磷和氧气点燃生成五氧化二磷,方程式为 4P+5O2 ![]() 2P2O5 ,B中碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,C中氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,氢氧化钡和稀硫酸反应生成硫酸钡和水,因此天平保持平衡的是ACD;
2P2O5 ,B中碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,C中氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,氢氧化钡和稀硫酸反应生成硫酸钡和水,因此天平保持平衡的是ACD;
(2) 将B、C实验的废液(含C中的蓝色沉淀)混合,得到蓝色沉淀及无色溶液,说明C中剩余氯化铜,B中剩余碳酸钠,氯化铜和碳酸钠反应生成碳酸铜和氯化钠,因此反应后的滤液中可能含有碳酸钠和氯化钠
(3)测定溶液pH时, 用玻璃棒沾取待测液滴到pH试纸上 , 然后与标准比色卡比较
步骤② 是碳酸钠和氯化钙反应生成碳酸钙和氯化钠,方程式为 Na2CO3+CaCl2=CaCO3↓+2NaCl
由于产生了白色沉淀,因此根据步骤①,可确定无色滤液的溶质除了NaCl外还含有碳酸钠, 如果步骤④的结果是溶液pH=11,则溶液C除了NaCl外含有的溶质是 氢氧化钠, 结合步骤①可确定猜想 IV 成立;
【分析】(1)根据林和氧气点燃生成五氧化二磷及各装置中发生的反应分析
(2)根据两支试管中含有的物质及发生的反应分析
(3)根据测定溶液pH的方法是碳酸钠和和氯化钙反应生成碳酸钙和氯化钠分析



 五氧化二磷
五氧化二磷