用化学用语填空:
( 1 )氟元素 ______ 。
( 2 ) 2 个铝原子 ______ 。
( 3 )葡萄糖( C 6 H 12 O 6 )在酶的催化作用下,与氧气反应可生成二氧化碳和水,该反应的化学方程式是 ______ 。
F 2Al
【详解】
( 1 )氟元素表示为: F ;
( 2 )原子用元素符号表示,多个原子就是在元素符号前面加上相应的数字,故 2 个铝原子表示为: 2Al ;
( 3 )葡萄糖在酶的催化作用下,与氧气反应可生成二氧化碳和水,该反应的化学方程式是: 。
化学发展史上,中国科学家取得了很多伟大成就。
( 1 )国际标准贡献者:张青莲教授主持测定了铟的相对原子质量的新值,被采用为国际新标准。铟元素的原子结构示意图和在周期表中信息如图所示。
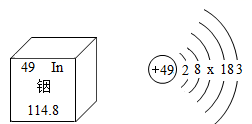
①图中 x= ______ ,铟原子形成的铟离子是 ______ (填符号)。
②铟位于元素周期表中第 ______ 周期,相对原子质量为 ______ 。
( 2 )磷的最早发现者:西汉刘安在《淮南子》中写到: “老槐生火,久血为磷。”描写的是磷自燃,请写出磷自燃的化学方程式 ______ 。
( 3 )制碱工业先驱者:侯德榜发明了 “侯氏联合制碱法”,其中一个反应是将碳酸氢钠煅烧生成纯碱、二氧化碳和水,该反应的化学方程式为 ______ 。
18 In 3+ 五 114.8
【详解】
( 1 ) ① 在原子中,质子数 = 核外电子数,故 49=2+8+ x +18+3 , x =18 ;
在元素周期表中,元素名称右上角的符号表示元素符号,故铟的元素符号为: In ,铟原子的最外层电子数为 3 ,小于 4 ,在化学反应中,容易失去最外层 3 个电子,从而带上 3 个单位的正电荷,形成铟离子为: In 3+ ;
② 铟原子核外有 5 个电子层,位于元素周期表中第五周期;
在元素周期表中,元素名称下方的数字表示相对原子质量,故铟的相对原子质量为 114.8 ;
( 2 )磷燃烧生成五氧化二磷,该反应的化学方程式为: ;
( 3 )碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,该反应的化学方程式为: 。
氯化钠是食盐的主要成分。电影《闪闪红星》讲述了潘东子给山上红军送盐的故事。
( 1 )藏盐:潘东子将食盐水吸在棉衣内给红军送盐。每人每天约需 3 — 5g 食盐,假设潘东子的棉衣可吸 1000g 水配成的食盐水,则 3℃ 时潘东子上山一次所携带的食盐,最多可以满足 ______ 名红军战士一天所需( 3℃ 时,氯化钠的溶解度约为 35.7g )。
( 2 )取盐:为取出食盐,潘东子将吸有食盐的棉衣放进水里,揉一揉,搓一提,其目的是 ______ 。然后,把得到的 “水”倒进锅里煮干,这种获得食盐的方法是 ______ 。
119 加快溶解速率 蒸发结晶
【详解】
( 1 ) 3℃ 时,氯化钠的溶解度约为 35.7g ,故该温度下, 1000g 水中可溶解 357g ,故最多可满足 357g÷3g=119 名红军战士一天所需;
( 2 )为取出食盐,潘东子将吸有食盐的棉衣放进水里,揉一揉,搓一提,其目的是加快溶解速率;
把得到的 “ 水 ” 倒进锅里煮干,这种获得食盐的方法是:蒸发结晶。
大量实验证明,化学反应符合质量守恒定律。
( 1 )如图是铁钉与硫酸铜溶液反应的实验。
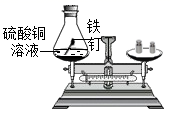
①反应一段时间,观察到的现象是 ______ 。
②该反应的化学方程式是 ______ 。
③溶液中减少的铜元素质量等于反应生成的 ______ 的质量。
( 2 )取足量的铁、锌,各加入相同质量相同溶质质量分数的稀盐酸,完全反应后,铁、锌均有剩余,下列说法正确的是 ______ 。
A 生成氢气的质量相等 B 生成的氯化亚铁和氯化锌的质量相等
C 参加反应的铁和锌的质量相等 D 参加反应的稀盐酸中 HCl 的质量相等
( 3 )经计算 3g 镁和 100g 质量分数 7.3% 的盐酸充分反应可生成氢气 0.2g ,但经实验测生成氢气的质量大于 0.2g ,则可能的原因是过量的镁与 ______ 发生反应。
天平平衡、有红色固体析出,溶液由蓝色变为浅绿色 铜 AD 水
【详解】
( 1 ) ① 铁与硫酸铜反应生成硫酸亚铁和铜,反应一段时间,观察到的现象是:天平平衡、有红色固体析出,溶液由蓝色变为浅绿色;
② 铁与硫酸铜反应生成硫酸亚铁和铜,故该反应的化学方程式是: ;
③ 根据质量守恒定律,化学反应前后,元素的种类和质量不变,故溶液中减少的铜元素质量等于反应生成的铜的质量;
( 2 ) A 、金属过量,酸不足,加入酸的质量和溶质质量分数相同,反应生成氢气的质量与酸中氢元素的质量相同,故最后生成氢气的质量相等,符合题意;
B 、铁与稀盐酸反应: ,锌与稀盐酸反应:
,氯化亚铁的相对分子质量小于氯化锌,故生成的氯化亚铁的质量小于氯化锌,不符合题意;
C 、根据化学方程式可知,金属过量,酸不足,消耗相同质量的酸,由于铁的相对原子质量小,参加反应的铁质量小,不符合题意;
D 、酸不足,金属过量,稀盐酸完全反应,稀盐酸的质量和溶质质量分数相同,故参加反应的稀盐酸中 HCl 的质量相等,符合题意。
故选 AC ;
( 3 )镁和稀盐酸反应: ,参加反应的镁与 HCl 的质量比为: 24:73 ,故 100g 质量分数 7.3% 的盐酸消耗 2.4g 镁,生成 0.2g 氢气,实际结果,生成氢气的质量大于 0.2g ,根据质量守恒定律,化学反应前后,元素的种类不变,盐酸中除了氯化氢,还有水中含有氢元素,故可能是过量的镁与水发生反应。
金属的利用和保护
( 1 )如图利用了铜的物理性质是 ______ 。

( 2 )如图说明铁具有 ______ 性。

( 3 )工业上利用一氧化碳和氧化铁炼铁的化学方程式是 ______ 。
( 4 )如图是用三枚洁净无锈铁钉探究铁生锈条件的实验。只有甲中铁钉有明显锈迹。

①实验乙中植物油的作用是 ______ 。
②由实验甲、丙可得出的结论是 ______ 。
( 5 )宜昌三峡机场新国际航站楼钢网架建设中,使用了 700 多吨钢。
①酸雨会腐蚀钢网架,造成酸雨的主要物质是 ______ 。
A 甲烷 B 二氧化硫 C 二氧化氮 D 一氧化碳
②钢网架防腐漆施工时规定,表面清理结束 4 — 8 小时内必须进行防腐底漆的喷涂,其原因是 ______ 。
导电性 导热 防止空气中的氧气溶于水 铁生锈需要与水接触 BC 隔绝氧气和水,防锈
【详解】
( 1 )铜制导线利用了铜的导电性;
( 2 )铁制炒锅,说明铁具有导热性;
( 3 )一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为: ;
( 4 ) ① 实验乙中植物油的作用是:防止空气中的氧气溶于水;
② 实验甲中铁钉与氧气和水接触,生锈,丙中铁钉只和氧气接触,不生锈,说明铁生锈需要与水接触;
( 5 ) ① 二氧化硫、二氧化氮能与水反应生成酸,导致酸雨。
故选 BC ;
② 进行防腐底漆的喷涂,可以隔绝氧气和水,起到防锈的目的。
本卷还有18题,登录并加入会员即可免费使用哦~

该作品由: 用户杨玉华分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。