大量实验证明,化学反应符合质量守恒定律。
( 1 )如图是铁钉与硫酸铜溶液反应的实验。
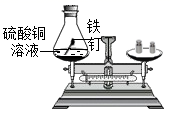
①反应一段时间,观察到的现象是 ______ 。
②该反应的化学方程式是 ______ 。
③溶液中减少的铜元素质量等于反应生成的 ______ 的质量。
( 2 )取足量的铁、锌,各加入相同质量相同溶质质量分数的稀盐酸,完全反应后,铁、锌均有剩余,下列说法正确的是 ______ 。
A 生成氢气的质量相等 B 生成的氯化亚铁和氯化锌的质量相等
C 参加反应的铁和锌的质量相等 D 参加反应的稀盐酸中 HCl 的质量相等
( 3 )经计算 3g 镁和 100g 质量分数 7.3% 的盐酸充分反应可生成氢气 0.2g ,但经实验测生成氢气的质量大于 0.2g ,则可能的原因是过量的镁与 ______ 发生反应。
答案
天平平衡、有红色固体析出,溶液由蓝色变为浅绿色 铜 AD 水
【详解】
( 1 ) ① 铁与硫酸铜反应生成硫酸亚铁和铜,反应一段时间,观察到的现象是:天平平衡、有红色固体析出,溶液由蓝色变为浅绿色;
② 铁与硫酸铜反应生成硫酸亚铁和铜,故该反应的化学方程式是: ;
③ 根据质量守恒定律,化学反应前后,元素的种类和质量不变,故溶液中减少的铜元素质量等于反应生成的铜的质量;
( 2 ) A 、金属过量,酸不足,加入酸的质量和溶质质量分数相同,反应生成氢气的质量与酸中氢元素的质量相同,故最后生成氢气的质量相等,符合题意;
B 、铁与稀盐酸反应: ,锌与稀盐酸反应:
,氯化亚铁的相对分子质量小于氯化锌,故生成的氯化亚铁的质量小于氯化锌,不符合题意;
C 、根据化学方程式可知,金属过量,酸不足,消耗相同质量的酸,由于铁的相对原子质量小,参加反应的铁质量小,不符合题意;
D 、酸不足,金属过量,稀盐酸完全反应,稀盐酸的质量和溶质质量分数相同,故参加反应的稀盐酸中 HCl 的质量相等,符合题意。
故选 AC ;
( 3 )镁和稀盐酸反应: ,参加反应的镁与 HCl 的质量比为: 24:73 ,故 100g 质量分数 7.3% 的盐酸消耗 2.4g 镁,生成 0.2g 氢气,实际结果,生成氢气的质量大于 0.2g ,根据质量守恒定律,化学反应前后,元素的种类不变,盐酸中除了氯化氢,还有水中含有氢元素,故可能是过量的镁与水发生反应。



 五氧化二磷
五氧化二磷