垃圾分类有利于保护环境,充分利用资源。某厂从废旧电子产品中回收贵重金属同时制备 CuSO 4 ·5H 2 O 的工艺流程如下:
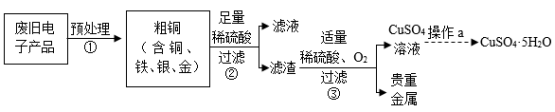
已知:步骤 3 中发生反应的化学方程式为: 。
回答下列问题:
(1) 从垃圾分类的角度,该厂加工的废旧电子产品属于 。
A .有害垃圾 B .可回收垃圾 C .厨余垃圾 D .其他垃圾
(2) 流程中步骤 ③ 回收的贵重金属为 _______ 。
(3) 流程中操作 a 表示一系列的操作,包括:蒸发浓缩、 _______ 、过滤、洗涤、干燥等。
(4) 步骤 ② 中发生反应的化学方程式为 _______ 。
答案
(1)B
(2) 金、银
(3) 降温结晶
(4)
【详解】( 1 )根据该流程图可知,可从废旧电子产品中回收贵重金属,同时制备 CuSO 4 ·5H 2 O ,于是从垃圾分类的角度,该厂加工的废旧电子产品属于可回收垃圾,故选 B ;
( 2 )根据流程中步骤 ② 是铁与稀硫酸反应生成硫酸亚铁和氢气,步骤 ③ 是铜与稀硫酸、氧气在加热条件下生成硫酸铜和水,所以粗铜中的铜和铁均已完全反应完,则流程中步骤 ③ 回收的贵重金属为金、银;
( 3 )由溶液得到晶体,应进行一系列的操作,包括:蒸发浓缩、降温结晶、过滤、洗涤、干燥等,故填:降温结晶;
( 4 )步骤 ② 中发生反应是铁与稀硫酸反应生成硫酸亚铁和氢气,该化学反应方程式为: ,故填:
。

 Cu+H2O
Cu+H2O 2Fe+3H2O
2Fe+3H2O 2Cu+CO2↑
2Cu+CO2↑ 4Fe+3CO2↑
4Fe+3CO2↑