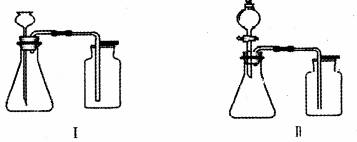茶垢清洁剂能快速清除茶具上附着的茶垢,某小组同学对茶垢清洁剂进行了探究。
〖查阅资料〗如图所示是某品牌茶垢清洁剂说明书中的部分内容。说明书中碳酸钠的俗称有误,应改为 _____ 。

〖提出问题 Ⅰ〗茶垢清洁剂溶于水时生成过氧化氢,是否生成氧气?
〖实验 1 〗在盛有茶垢清洁剂固体的小烧杯中,加适量常温水,完全溶解后得到无色溶液,观察到有小气泡缓慢冒出,伸入带火星的木条,木条不复燃。
〖实验 2 〗取三份等量的实验 1 中的溶液,分别加入甲、乙、丙三支试管中,按图所示进行实验。观察到都较快产生气泡,且温度越高产生气泡越快;伸入带火星的木条,木条都复燃。
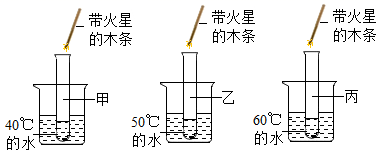
〖表达交流 Ⅰ〗通过实验证明,茶垢清洁剂溶于水时生成氧气。
(1) 实验 1 中 “ 木条不复燃 ” 的原因是 _______ 。
(2) 实验 2 中丙试管内不再产生气泡后,其中溶液所含溶质与加热前溶液的不同是 _______ 。
〖提出问题 Ⅱ〗茶垢清洁剂溶于水时生成碳酸钠,是否生成氢氧化钠?
〖实验 3 〗取实验 2 丙试管内溶液,按如图流程进行实验。
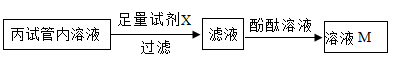
〖表达交流 Ⅱ〗
(1) 加入试剂 X 的目的是 _______ ( 用化学方程式表示 ) 。
(2) 不新增试剂,检验加入的试剂 X 已足量的方法是 _______ 。
(3) 溶液 M 呈 _______ 色,说明茶垢清洁剂溶于水时没有生成氢氧化钠。
〖反思总结〗
(1) 茶垢清洁剂溶于水生成了碳酸钠和过氧化氢。碳酸钠溶液有较好的去污效果,过氧化氢分解生成活性氧,可深层带走污垢。
(2) 使用茶垢清洁剂时应选择 _______ 的水进行溶解,去垢效果更好。
答案
纯碱或苏打 产生氧气速率较慢,氧气浓度过低,不足以使带火星木条复燃 无过氧化氢
取少量滤液于试管中,滴加 Na 2 CO 3 溶液,若有白色沉淀生成,说明试剂 X(CaCl 2 ) 过量 无色 硬度较小
【详解】
查阅资料 1 :碳酸钠俗称苏打、纯碱;
表达交流 Ⅰ :( 1 )实验 1 中 “ 木条不复燃 ” 的原因是常温下过氧化氢的分解速率很慢,产生氧气的速率慢,氧气浓度低,不足以使带火星的木条复燃;
( 2 )过氧化氢受热分解生成水和氧气,故实验 2 中丙试管内不再产生气泡后,其中溶液所含溶质与加热前溶液的不同是无过氧化氢;
表达交流 Ⅱ :( 1 )由于溶液中存在碳酸钠,碳酸钠显碱性,也能使无色酚酞试液变红,会影响氢氧化钠的检验,故加入的试剂 X 可以是氯化钙,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,可将碳酸钠除尽,该反应的化学方程式为: ;
( 2 )氯化钙能与碳酸钠反应生成碳酸钙沉淀和氯化钠,产生白色沉淀,故取少量滤液于试管中,滴加 Na 2 CO 3 溶液,若有白色沉淀生成,说明试剂 X(CaCl 2 ) 过量;
( 3 )说明茶垢清洁剂溶于水时没有生成氢氧化钠,则溶液显中性,不能使无色酚酞试液变色,故溶液 M 呈无色;
反思总结:( 2 )使用茶垢清洁剂时应选择硬度较小的水进行溶解,去垢效果更好,否则硬水中的可溶性含钙化合物可能与碳酸钠反应,消耗碳酸钠。

 K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑
 2H2O+O2↑
2H2O+O2↑