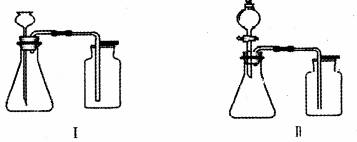某化学兴趣小组对 “ 氧化铜能否作过氧化氢分解的催化剂 “ 进行了探究
(实验探究)
| 实验编号 | 实验操作 | 实验现象 | 实验分析或结论 | |
| 实验分析 | 实验结论 | |||
| ① | | 有少量气泡;木条不复燃 | 过氧化氢能分解,但是 _________ | 氧化铜是过氧化氢分解的催化剂 |
| ② | | __________________ | 氧化铜能加快过氧化氢分解 | |
( 1 )写出实验 ②中反应的化学方程式: ___________________ 。
(交流反思)实验过程中加入到两支试管里的过氧化氢溶液应满足的要求有 _________________ 。
①体积相同 ②浓度相同 ③温度相同
( 2 )小明同学认为仅由上述实验还不能完全得出表内的 “ 总结 ” ,他补充设计了以下两个探究实验
实验一:称量反应后固体质量,并与反应前的称量数据作比较,其目的是 ________________ 。
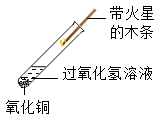
实验二:另取 5mL5% 的过氧化氢溶液于试管中,再向其中加入实验 ②反应后的固体剩余物,如图 1 所示,其目的是证明 _______________________ 。
(实验拓展)小红同学用 MnO 2 、 CuO 两种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球探究分解过氧化氢溶液制取氧气的适宜催化剂。
实验操作:取 30 粒含 MnO 2 的海藻酸钠微球,采用图 1 装置进行实验。改用另一种微球,分别重复上述实验,得到图 2 的锥形瓶内压强随时间变化的曲线图。
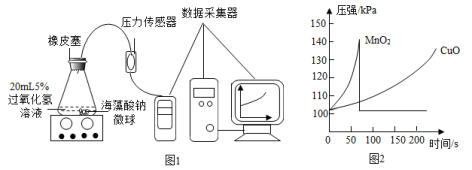
( 3 )每次实验时,海藻酸钠微球数应相同的原因是 _____________ 。
( 4 )用含 MnO 2 的海藻酸钠微球进行实验, 60s 时压强瞬间回落,其原因是 _______________ 。
( 5 )从实验曲线看,催化效果较好、反应温和的催化剂是 __________________ 。
答案
反应速度太慢 有大量气泡产生,带火星的木条复燃 2H 2 O 2 2H 2 O+O 2 ↑ ①② 证明反应前后氧化铜的质量不变 反应后氧化铜的化学性质不变 为了加入质量相等的催化剂,确保催化剂用量一致 产气速率过快,导致气压过大,橡胶塞被弹出 CuO
【详解】
实验探究:过氧化氢能分解,但是分解的速率太慢,故带火星的木条不复燃;故填:反应速度太慢;氧化铜能加快过氧化氢的分解,故可以在试管中加入氧化铜,设计实验要注意控制变量,过氧化氢与实验 ①中的要一样,反应后观察到产生气泡速度快,且带火星的木条复燃,故填:有大量气泡产生,带火星的木条复燃;
( 1 )实验 ②中过氧化氢在氧化铜的催化作用下分解生成水和氧气,反应的化学方程式为: 2H 2 O 2 2H 2 O+O 2 ↑ ;
交流反思:
实验过程中加入到两支试管里的过氧化氢溶液应满足的要求有浓度、体积完全相同;
( 2 )要证明氧化铜是反应的催化剂,还需要证明反应前后氧化铜的质量和化学性质不变;( 3 )每次实验时,海藻酸钠微球数应相同的原因是为了加入催化剂的质量相等。故填:为了加入质量相等的催化剂,确保催化剂用量一致。
( 4 )用含 MnO 2 的海藻酸钠微球进行实验, 60s 时压强瞬间回落,原因是产气速率过快,导致气压过大,橡胶塞被弹出;
( 5 )从实验曲线看,催化效果较好、反应温和的催化剂是氧化铜( CuO )。


 K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑
 2H2O+O2↑
2H2O+O2↑