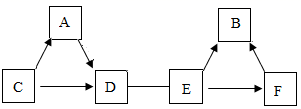
用 A 、 B 、 C 、 D 、 E 、 F 分别代表六种纯净物,它们的部分反应和转化关系如下图( “—” 表示两种物质能发生反应, “→” 表示一种物质能转化成另一种物质,且省略部分反应物或生成物及条件)。其中 A 、 C 、 D 是生活中常见的气体, A 、 D 是氧化物, C 是单质。 E 、 B 、 F 是固体单质, E 为黑色,可用于冶金工业; B 为紫红色; F 为银白色,它是最常见的金属。问:
( 1 )写出 A 、 C 的化学式: A_______ ; C_______ ;
( 2 )写出 F→B 发生化学反应的现象 ___________________________ ;
( 3 )写出 D 与 E 发生反应的化学方程式为 ____________________________ 。
答案
CO ;; O 2 ; 银白色物质表面有红色物质析出,溶液由蓝色变为 ( 浅 ) 绿色; CO 2 +C ![]() 2CO ;
2CO ;
【分析】
A 、 C 、 D 是生活中常见的气体, A 、 D 是氧化物, C 是单质。结合图中转化关系可知, C 是氧气, A 是一氧化碳, D 是二氧化碳,碳和氧气发生不完全燃烧反应生成一氧化碳,完全燃烧生成二氧化碳,一氧化碳和氧气在点燃条件下反应生成二氧化碳; E 、 B 、 F 是固体单质, E 为黑色,可用于冶金工业且能与二氧化碳反应;可知 E 为碳,碳和氧化铜高温条件下反应生成铜和二氧化碳,碳和二氧化碳高温下反应生成一氧化碳,铜是紫红色金属, B 为铜; F 为银白色,它是最常见的金属, F 是铁,铁和硫酸铜溶液反应生成铜和硫酸亚铁。
【详解】
( 1 )化学式: A : CO ; C : O 2 ;
( 2 ) F→B 即铁和硫酸铜发生化学反应的现象银白色物质表面有红色物质析出,溶液由蓝色变为 ( 浅 ) 绿色;
( 3 )碳和二氧化碳发生反应的化学方程式为: CO 2 +C ![]() 2CO 。
2CO 。
【点睛】
推断题的解题方法是找题眼,物质颜色、用途等,然后结合转化关系,利用反应条件和反应类型,进行推断,最后再将推断的结果检查,看是否符合题中物质间的关系。

 Cu + H2O。
Cu + H2O。 
 H2O+Cu
H2O+Cu