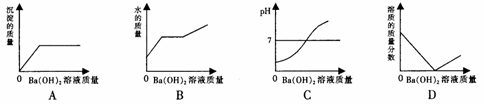
某化学课外活动小组的同学在学习《化学》下册 77 页的资料卡片 “ 石笋和钟乳石的形成 ” 时,发现难溶于水的 CaCO 3 当遇到溶有 CO 2 的水时,会反应生成溶解性较大的 Ca(HCO 3 ) 2 ( CaCO 3 +CO 2 +H 2 O= Ca(HCO 3 ) 2 )。联想到实验室检验 CO 2 时,是将气体通入澄清石灰水中。若长时间往澄清石灰水中通入 CO 2 会产生什么样的现象呢?小组决定用小烧杯盛装一定量的氢氧化钠溶液并不断通入二氧化碳气体进行探究。
(提出问题)氢氧化钠溶液中通入二氧化碳一段时间后,溶液中会有什么溶质?
(查阅资料)
(1) 通入少量的二氧化碳时, NaOH 与 CO 2 反应的化学方程式 _____________ 。
(2) 通入过量的二氧化碳时,反应的化学方程式为 Na 2 CO 3 +CO 2 +H 2 O= 2NaHCO 3
(3) 碳酸氢盐都能溶于水, BaCO 3 难溶于水且是白色固体。
(4)Na 2 CO 3 、 NaHCO 3 的溶液呈碱性、 BaCl 2 呈中性
(提出猜想) (1) 溶质有 NaOH、Na 2 CO 3 ; (2) 溶质为 Na 2 CO 3 ; (3) 溶质是 ________ ( 填化学式 );(4) 溶质全部是 NaHCO 3
(设计实验方案)
| 实验步骤 | 实验现象 | 实验结论 |
| ①用试管取少量小烧杯中反应后的溶液,滴加几滴 ______ 试液 ( 填酸碱指示剂 ) | 溶液变红色 | 该溶液显碱性 |
| ②将小烧杯中反应后剩下的溶液进行称量,然后滴加过量的 BaCl 2 溶液 | 有 _______ 生成 | 猜想 (4) 不成立 |
| ③取步骤②静置后的上层清液,滴入稀盐酸 | 有气泡冒出 | 猜想 (1) 和 (2) 不成立 |
(得出结论)猜想 (3) 成立
(讨论交流)
(1) 有同学提出实验步骤 ①是多余的。你认为该实验设计是否需要?并说明理由 ___________ 。
(2) 将实验步骤 ②剩下混合物进行 _______ ( 填操作名称 ) 、洗涤、干燥、称量。发现所得沉淀质量等于步骤 ②中所称量的溶液质量的十分之一,判断氢氧化钠溶液中通入二氧化碳一段时间后,溶液中 Na 2 CO 3 的质量分数约为 ( ______ )
A.4.26% B.5.38% C.3.43% D.10%
(反思应用)
验证二氧化碳性质时,如果长时间向澄清石灰水中通入二氧化碳会看到什么样的现象呢?请你描述一下: _________________ 。
答案
2NaOH+CO 2 =Na 2 CO 3 +H 2 O Na 2 CO 3 、 NaHCO 3 酚酞 白色沉淀 ( 或白色固体 ) 不需要。理由是 NaOH 溶液、 Na 2 CO 3 溶液、 NaHCO 3 溶液都显碱性 过滤 B 澄清石灰水变浑浊,再慢慢变澄清
【详解】
【 查阅资料 】 通入少量的二氧化碳时, NaOH 与 CO 2 反应的化学方程式为 2NaOH+CO 2 =Na 2 CO 3 +H 2 O ; 提供的信息可知,溶液中的溶质可能是氢氧化钠和碳酸钠;碳酸钠;碳酸氢钠和碳酸钠;碳酸氢钠等情况;据题中的结论可知, ① 用试管取少量小烧杯中反应后的溶液,滴加几滴酚酞试液,溶液变红色,说明溶液显碱性; ② 将小烧杯中反应后剩下的溶液进行称量,然后滴加过量的 BaCl 2 溶液,产生白色沉淀,说明猜想四不成立;
【 讨论交流 】 步骤 ① 是多余的理由为是 NaOH 液、 Na 2 CO 3 溶液、 NaHCO 3 溶液都显碱性;
( 2 )将实验步骤 ② 剩下混合物进行过滤,假设生成碳酸钡的质量为 197g ;根据化学方程式
得到碳酸钠的质量为 106g ,溶液的质量为 1970g ,故溶液中 Na 2 CO 3 的质量分数约为 106g/1970g×100%=5.38% ;
【 反思应用 】 验证二氧化碳性质时,如果长时间向澄清石灰水中通入二氧化碳会看到的现象为澄清石灰水变浑浊,再慢慢变澄清,因为碳酸钙会继续与二氧化碳和水反应生成可溶于水的碳酸氢钙。