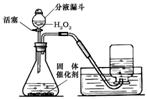
工业上用闪锌矿(主要含ZnS,还含PbS等杂质)制备锌的流程如下(部分产物略去):
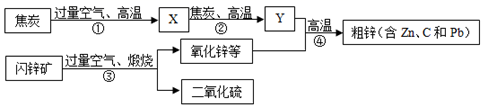
(1)X的化学式是_______, 图中用过量空气的目的是_________ 。
(2)①~④中属于化合反应的是______。
(3)Zn______(填“能”或“不能 )与PbCl2溶液反应。
(4)写出反应③中生成ZnO的化学方程式_________。
(5)结合下表数据设计:从粗锌中分离出纯锌的方案是_________。
| 物质 | Zn | Pb | C |
| 沸点℃ | 907 | 1749 | 4827 |
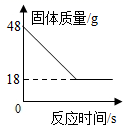
(6)反应②中固体质量随反应时间的变化图示如下图,计算产生Y的质量__________。(写出必要的计算过程)
答案
CO2 使焦炭完全反应 ①② 能 2ZnS+3O2![]() 2ZnO+2SO2 将粗锌放在一容器中高温(保持温度907-1749℃),收集的锌蒸汽,冷却后可得纯净的锌 140g
2ZnO+2SO2 将粗锌放在一容器中高温(保持温度907-1749℃),收集的锌蒸汽,冷却后可得纯净的锌 140g
【解析】
(1)焦炭在高温的条件下与过量的空气反应生成二氧化碳,故X的化学式为CO2 题中用过量的空气是使焦炭完全反应;
(2)①是碳与氧气反应生成二氧化碳,是化合反应,②是碳与二氧化碳反应生成一氧化碳,故是化合反应,反应③是硫化锌与氧气反应生成氧化锌和二氧化硫,不是化合反应,反应④是一氧化碳还原氧化锌,不是化合反应,故选①②;
(3)在金属活动性顺序中,锌比铅活泼,故Zn能与PbCl2溶液反应;
(4)反应③是硫化锌与氧气反应生成氧化锌和二氧化硫,反应方程式为2ZnS+3O2![]() 2ZnO+2SO2;
2ZnO+2SO2;
(5)由于锌在907-1749℃的范围内有固态变为气态,而铅不会,故从粗锌中分离出纯锌的方案是将粗锌放在一容器中高温(保持温度907-1749℃),收集的锌蒸汽,冷却后可得纯净的锌
(6)由图可知,参加反应的碳的质量为48g-18g=30g,设生成一氧化碳的质量为x
CO2 + C 高温 2CO
12 56
30g x
![]() =
=![]() ,解得x=140g
,解得x=140g
答:产生Y的质量为140g。