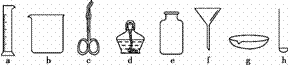
根据所学化学知识回答问题。
(1)在粗盐提纯的实验中其主要的操作步骤顺序是__(填数字序号)。
①过滤
②溶解
③蒸发
④计算产率
(2)在蒸发加热过程中,应用玻璃棒不断搅拌,防止因局部温度过高,造成___;当蒸发皿中出现_时,应停止加热。
(3)欲除去粗盐中可溶性杂质Na2SO4、MgCl2、 CaCl2 得到纯净的NaCl,所加试剂为稍过量的BaCl2溶液、稍过量的___ (填化学式) 溶液、稍过量的Na2CO3溶液和适量的稀盐酸。
(4)纯净的氯化钠是重要的化工产品,熔融态的氯化钠通电可生成金属钠和氯气,写出该反应的化学方程式__。
答案
②①③④ 液体飞溅 大量固体 NaOH 2NaCl![]() 2Na+Cl2↑
2Na+Cl2↑
【详解】
(1)在粗盐提纯的实验中其主要的操作步骤顺序是:先溶解粗盐,然后过滤(除去粗盐中的不溶性物质)再蒸发结晶,得到氯化钠晶体,最后计算产率;
正确的操作顺序:②①③④;
(2)在蒸发加热过程中,应用玻璃棒不断搅拌,防止因局部温度过高,造成液体飞溅;当蒸发皿中出现大量固体时,应停止加热,用余热蒸干。
(3)欲除去粗盐中可溶性杂质Na2SO4、MgCl2、 CaCl2 得到纯净的NaCl,所加试剂为稍过量的BaCl2溶液(用于除去硫酸根离子)、稍过量的氢氧化钠(NaOH)溶液(用于除去镁离子)、稍过量的Na2CO3(用于除去钙离子和过量的钡离子)溶液和适量的稀盐酸(用于除去过量的碳酸根离子和氢氧根离子)。
(4)纯净的氯化钠是重要的化工产品,熔融态的氯化钠通电可生成金属钠和氯气,写出该反应的化学方程式2NaCl![]() 2Na+Cl2↑。
2Na+Cl2↑。


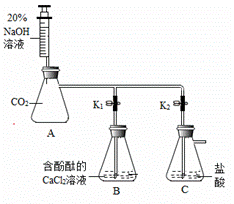
 B
B
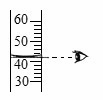 D
D