某化学兴趣小组在实验室里验证二氧化碳的某些性质。
(实验设计)甲同学设计了如下图所示装置。
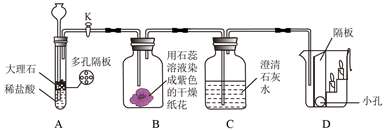
(讨论交流)该小组同学对该装置进行了讨论,提出意见如下:
(1)乙同学认为 B 中纸花是干燥的,二氧化碳不能使其变红。
(2)丙同学认为二氧化碳会被澄清石灰水吸收,D 中蜡烛不会熄灭。
(现象分析)当打开 K,反应一段时间后:
(1)与乙同学的预测不一致,B 中干燥纸花变红,原因是_________________________ 。
(2)C 中澄清石灰水变浑浊,该反应的化学方程式是_____________________________ 。
(3)与丙同学的预测不一致,D 中蜡烛熄灭,请从溶解性的角度说明澄清石灰水不能完全 吸收二氧化碳的原因:___________________________。
(4)D 中__________________________ (填“上层”或“下层”)的蜡烛先熄灭,说明二氧化碳具有的物理性 质是__________________________ ,具有的化学性质是___________________________。
(查阅资料)自然温室气体包括水蒸气,水蒸气所产生的温室效应大约占整体温室效应的
60~70%,其次是二氧化碳大约占 26%,其他还有臭氧、甲烷、氟氯代烷等。
(拓展探究)该小组同学利用温度传感器验证二氧化碳和水蒸气是温室气体。用集气瓶收集 相同体积的三种气体样本(分别是干燥的二氧化碳、湿润的二氧化碳和干燥的空气),经太 阳灯光源等距离照射,得到温度随时间变化的曲线(如下图)。
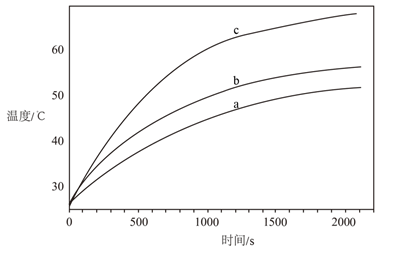
(得出结论)通过曲线 a 和 b 的对比,可以得出二氧化碳是温室气体的结论;通过曲线 b 和c 的对比,可以得出水蒸气是温室气体的结论。则曲线 a、b、c 对应的气体样本依次是_______________________
答案
生成的气体从溶液中逸出时会带出水 Ca(OH)2+CO2=CaCO3↓+H2O 常温下,氢氧化钙微溶于水,因此澄清石灰水中含有的 Ca(OH)2 很少,因此澄清石灰水无法完全吸收二氧化碳; 下层 相同条件下二氧化碳密度比空气大 不燃烧也不支持燃烧 a对应干燥的空气,b对应干燥的二氧化碳,c对应湿润的二氧化碳;
【详解】
(1)B中干燥纸花变红,原因是气体通过溶液时会带出水蒸气;故答案为生成的气体从溶液中逸出时会带出水;
(2)二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;故答案为Ca(OH)2+CO2=CaCO3↓+H2O;
(3)从溶解性的角度说明澄清石灰水不能完全吸收二氧化碳的原因:常温下,氢氧化钙微溶于水,因此澄清石灰水中含有的 Ca(OH)2 很少,因此澄清石灰水无法完全吸收二氧化碳;故答案为常温下,氢氧化钙微溶于水,因此澄清石灰水中含有的 Ca(OH)2 很少,因此澄清石灰水无法完全吸收二氧化碳;
(4)D中下层的蜡烛先熄灭,说明二氧化碳具有的物理性质是:相同条件下二氧化碳密度比空气大;具有的化学性质是:不燃烧也不支持燃烧;故答案为下层;相同条件下二氧化碳密度比空气大;不燃烧也不支持燃烧;
【得出结论】
按照控制变量的方法,a、b对照得出二氧化碳是温室气体的结论,图中b气体温度高于a,因此a是干燥的空气,b是干燥的二氧化碳;b、c 对照得出水蒸气是温室气体的结论,b是干燥的二氧化碳,因此c是湿润的二氧化碳;故答案为a对应干燥的空气,b对应干燥的二氧化碳,c对应湿润的二氧化碳;

 2Fe + 3CO2
2Fe + 3CO2 