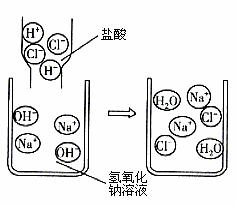
(2019·江西)化学实验社团在老师的指导下开展了“模拟酸雨形成”的相关实验。
(联想与实验)模仿二氧化碳与水反应进行如图一所示实验:
资料卡片
1.二氧化硫与二氧化碳的化学性质相似,能与水反应生成亚硫酸(H2SO3),亚硫酸也不稳定。
2.整个实验在通风橱中进行。
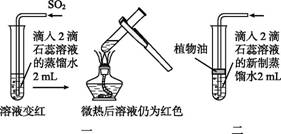
(问题与猜想)亚硫酸不稳定,为什么红色液体微热后不变为紫色?其原因可能为:
猜想1:加热不够充分;
猜想2:与空气中氮气有关;
猜想3:与空气中氧气有关。
(探究与验证)填写表格中的空格。
| 编号 | 操作 | 现象 | 结论 |
| 1 | 将图一中红色液体继续加热至沸腾 | 仍为红色 | 猜想1 不成立 |
| 2 | 如图二所示,先通入适量SO2,然后用酒精灯微热 | 先变红 后变紫 | 猜想2 不成立 |
| 3 | 如图二所示,先通入适量SO2,再改通入氮气,最后用酒精灯微热 |
| |
| 4 | 如图二所示,先通入适量SO2,再改通入 ,最后用酒精灯微热 |
| 猜想3 成立 |
(分析与结论)红色液体微热后不变为紫色的原因是:H2SO3在空气中会被氧化生成另一种酸,进一步实验证明是硫酸。
(应用与拓展)收集某硫酸厂(生产过程中产生SO2)附近刚降到地面的雨水水样,用pH计测得每隔十分钟数据如下表:
| 测定时间 | 5:05 | 5:15 | 5:25 | 5:35 | 5:45 |
| pH | 4.95 | 4.94 | 4.86 | 4.85 | 4.85 |
(1)分析表中数据,5:15至5:25时间段内水样中主要酸性溶质有 。
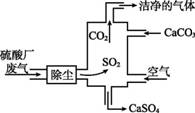
(2)实验社团提出一种处理废气的方案如图,利用CaCO3粉末、空气为原料,在高温下吸收SO2,写出该反应的化学方程式:
。
答案
(探究与验证)先变红后变紫 氧气(或O2) 先变红色,微热后仍为红色
(应用与拓展)(1)H2SO3和H2SO4
(2)2CaCO3+O2+2SO2![]() 2CaSO4+2CO2
2CaSO4+2CO2
解析:(探究与验证)根据猜想2不成立可知,溶液变色情况与空气中的氮气无关,所以通入氮气后再加热,现象是先变红后变紫;根据猜想三成立,则说明溶液变色情况与空气中的氧气有关,操作中应通入氧气,氧气可以与亚硫酸反应生成硫酸,硫酸的稳定性强于亚硫酸,所以加热后仍为红色。(应用与拓展)(1)因为5:15至5:25时间段内水样的pH在逐渐减小,说明亚硫酸还未完全转化为硫酸,所以此时水样中主要酸性溶质有亚硫酸和硫酸。(2)碳酸钙与二氧化硫及空气中的氧气在高温下反应生成硫酸钙和二氧化碳气体。

 Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O
Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑