化学兴趣小组的同学们在老师的带领下走进实验室,开展实验活动。
(1)实验室依次编号为1、2、3、4的药品柜中,分别存放常见的酸、碱、盐和酸碱指示剂。小刚欲使用熟石灰,他需从_____号柜中取出。
(2)小涵发现盛放Na2CO3与NaCl两种溶液的试剂瓶标签脱落,为鉴别两种溶液,分别取样于试管中,加入无色酚酞溶液,若为Na2CO3,则观察到溶液变为____色。
(3)小文从柜中取出标有“10%NaOH溶液”的试剂瓶,取少量样品加入试管中,向其中滴入稀盐酸,发现产生气泡,判断该NaOH溶液中含有Na2CO3.用化学方程式表示NaOH溶液变质的原因:__________。
小文同学对变质的NaOH溶液进行如下一系列实验,实现药品再利用。
Ⅰ.测定NaOH溶液中有Na2CO3的质量分数
【实验操作】取40.0g10%的NaOH溶液样品进行如题所示的实验。
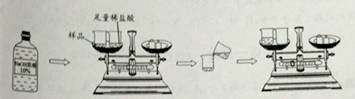
【数据处理】
①所取用盐酸(溶质质量分数7.3%)的质量理论上不少于____g。
②图中,反应前后天平示数相差1.1g,计算NaOH溶液中Na2CO3的质量分数(写出计算过程)。
Ⅱ.变质的NaOH溶液再利用
小文将剩余NaOH溶液倒入烧杯中,加入经计算所需的熟石灰粉末,充分搅拌,静置、过滤,得到NaOH溶液和滤渣,充分搅拌的主要目的是_______。
(4)实验结束后,同学们将实验产生的废液和废渣倒入指定的烧杯中,得到无色溶液和白色沉淀,溶液中除一定存在的溶质外,可能存在的溶质是________。
同学们再次实验,确认成分后,对废液回收利用,绿色排放。
答案
【答案】(1)2 (2)红 (3)2NaOH+CO2=Na2CO3+H2O
Ⅰ.①50.0
②解:NaOH溶液中Na2CO3的质量为x。
Na2CO3+2HCl=2 NaCl+H2O+CO2↑
106 44
x 1.1g
![]()
x=2.65g
NaOH溶液中Na2CO3的质量分数为![]() ×100%=6.6%。
×100%=6.6%。
答:NaOH溶液中Na2CO3的质量分数为6.6%。
Ⅱ.让溶液中的碳酸钠与熟石灰充分反应,完全除去
(4)CaCl2