1一些金属易生锈,某小组同学设计如下实验,对金属锈蚀进行探究。
[实验一] 取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验。
| 实验 图示 |
|
|
|
|
|
| 生锈 时间 | 8 min | 较长时间 不生锈 | 5 min | 3 min | 1 min |
(1)通过上述实验可知,温度越高,铁生锈速率越________(填“慢”或“快”);在__________(填“酸性”“碱性”或“中性”)环境中铁钉生锈速率较快。
[实验二] 为探究铁锈的成分,用如图Z3-28所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全)。
[查阅资料] 无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收CO2。
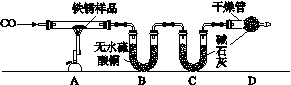
图Z3-28
(2)请指出上图所示实验装置的一个明显缺陷:______________________。
(3)加热前,先通入CO一段时间,目的是____________________________________。
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有________元素,从而推断出空气中的________参加了铁生锈反应。
[实验记录]
| 铁锈样品的质量/g | 装置B的质量/g | 装置C的质量/g | |
| 反应前 | 23.2 | 232.4 | 198.2 |
| 反应后 | / | 239.6 | 211.4 |
(5)根据上表数据推算,可确定铁锈的成分,用FexOy·nH2O表示,则n=________;若缺少D装置,x∶y的值________(填“偏大”“偏小”或“无影响”)。
[实验三] 镁带久置空气中,表面因锈蚀而变黑,此黑色物质是碱式碳酸镁(带结晶水的碳酸镁和氢氧化镁的混合物)。
(6) 欲通过如图Z3-29所示装置探究镁带在空气中锈蚀的条件,试管内可选用的物质如下:①O2,②水,③CO2,④O2和CO2,⑤CO2和水,⑥O2和水,⑦O2、CO2和水。至少需要选用________(填序号),才能达到探究镁带锈蚀的条件。
![]()
图Z3-29
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁[Mg3(OH)2(CO3)2]的化学方程式:________________________________________________________________________。
答案
(1)快 酸性 (2)没有尾气处理装置
(3)排尽玻璃管内的空气,防止爆炸
(4)氢(或H) 水 (5)4 偏小 (6)④⑤⑥⑦
(7)6Mg+4CO2+2H2O+3O2===2Mg3(OH)2(CO3)2