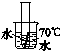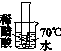分析图Z3-8,回答问题。

图Z3-8
(1)实验室用二氧化锰和氯酸钾制取氧气时,发生装置可以选用图①中装置________(填字母),二氧化锰作该反应的__________________。
(2)用图②的装置进行铁丝在氧气中燃烧的实验,容易导致集气瓶炸裂,为了避免这种情况,应采取的措施是________________________________________________________________________。
(3)如图③所示,红磷用酒精灯加热后才能燃烧,由此可知可燃物燃烧的条件之一是____________________________;红磷燃烧后冷却至室温,活塞a停在刻度________(填数字)处。
.(1)B 催化剂
(2)在集气瓶底部放少量水或铺一层细沙
(3)温度达到可燃物的着火点 8
[解析] (1)用氯酸钾与二氧化锰混合制氧气需要加热,故选用装置B;其反应中加二氧化锰是为了加快氯酸钾的分解速率,其质量和化学性质在反应前后不变。(2)铁在氧气中剧烈燃烧,火星四射,放出大量的热,为防止溅落的高温熔融物炸裂瓶底,需预先在集气瓶底部放少量水或铺一层细沙。(3)燃烧的条件:(缺一不可)①可燃物、②氧气(或空气)、③温度达到可燃物着火点。红磷需要加热才能燃烧,说明燃烧需要温度达到可燃物的着火点。由于空气中氧气体积大约占![]() ,从图③中可知,没点燃红磷前空气体积有10份,则氧气占2份,当足量红磷与氧气反应后,则将氧气消耗完,故冷却至室温后,活塞a应该停在刻度8处。
,从图③中可知,没点燃红磷前空气体积有10份,则氧气占2份,当足量红磷与氧气反应后,则将氧气消耗完,故冷却至室温后,活塞a应该停在刻度8处。
人体代谢产生的过氧化氢,对人体有毒害作用。人体肝脏中的过氧化氢酶能催化过氧化氢分解产生氧气和水。某同学查阅资料发现,FeCl3也能催化过氧化氢分解。为比较过氧化氢酶和FeCl3催化效率的高低,该同学在28 ℃环境下进行了如下探究:
(1)提出问题:过氧化氢酶和FeCl3催化效率哪个更高?
(2)猜想与假设:________________________________________________________________________。
(3)实验材料:适宜浓度的FeCl3溶液,适宜浓度的新鲜猪肝研磨液(含有过氧化氢酶),适宜浓度的过氧化氢溶液等。
(4)实验步骤:
①取2支洁净的试管,编号为1、2,并各注入3 mL适宜浓度的过氧化氢溶液;
②向1号试管内滴入适宜浓度的FeCl3溶液,向2号试管内________________________________________________________________________;
③观察并记录两支试管产生气泡的情况。

图Z3-16
(5)预测实验结果:
请写出一种可能的实验结果:________________________________________________________________________。
(6)在以上探究的基础上,该同学又完成了“探究温度对猪肝研磨液和FeCl3催化效率的影响”实验。实验结果如图Z3-16所示。图中代表猪肝研磨液催化效率的曲线是________,判断的理由是__________________________________________________________________________________________。
.(2)过氧化氢酶的催化效率更高(其他假设也可)
(4)滴加相同滴数适宜浓度的新鲜猪肝研磨液
(5)1号试管产生气泡的速率比2号试管快(或“慢”或“基本相等”)
(6)乙 酶的活性受温度影响,在一定范围内,随温度的升高,酶的活性增强;超过适宜的温度范围,酶的活性会随温度的升高而减弱
[解析] (2)猜想与假设有三种情况:①过氧化氢酶的催化效率更高;②FeCl3溶液的催化效率更高;③过氧化氢酶与FeCl3溶液的催化效率相当(任答一条即可)。(4)此题就是比较过氧化氢酶和FeCl3催化效率的高低,所以实验步骤是向1号试管内滴入适宜浓度的FeCl3溶液,向2号试管内滴加相同滴数适宜浓度的新鲜猪肝研磨液。(6)酶是有催化效果的蛋白质,而且酶的催化具有高效性,但是温度要适宜,若温度较高,蛋白质要发生变性,催化效果会降低。但温度对FeCl3的影响不大,且温度越高过氧化氢的分解速率会增加,所以代表猪肝研磨液催化效率的曲线是乙。
已知:CO2和SO2既有相似性也有差异性。请回答相关问题。
| 气体 | CO2 | SO2 | |
| 制剂 | 石灰石与盐酸 | Na2SO3与70%硫酸 | |
| 相似性 | 溶解性 | 能溶于水 | 易溶于水 |
| 与澄清石 灰水反应 | 二者都产生白色浑浊 | ||
| 差异性 | 与KMnO4 溶液 | 不反应 | 气体被吸收,溶液逐渐褪色 |
(1)化石燃料燃烧的气体产物中有CO2和SO2等物质,其中SO2是形成__________(填一污染名称)的主要物质。
(2)制取CO2的化学方程式是____________________________,可用于收集CO2的装置是__________(填图Z3-22中序号)。

图Z3-22
(3)写出Na2SO3与70%硫酸反应的化学方程式:________________________________________________________,
制备SO2的发生装置用__________(填序号)。
(4)将收集满SO2的试管倒扣在水中观察到的现象是________________________。
(5)结合已知信息,请你设计实验证明化石燃料燃烧的气体产物中有CO2(写出操作、试剂、现象、结论):________________________________________________________________________________________________________________________________________________________________________________________________________________________。
(1)酸雨
(2)CaCO3+2HCl===CaCl2+H2O+CO2↑ ②或③
(3)Na2SO3+H2SO4===Na2SO4+H2O+SO2↑
⑥
(4)水进入试管,液面上升
(5)操作:将化石燃料燃烧的气体先通入足量的KMnO4溶液中,再通入澄清石灰水中;试剂:KMnO4溶液、澄清石灰水;现象:KMnO4溶液变浅,澄清石灰水变浑浊;结论:化石燃料燃烧的气体产物中有CO2
金属材料的研究和应用是化学学习的一个重要内容。
(1)为了探究铁制品锈蚀的条件,做了如图Z3-27所示的3个对比实验,一周后,B、C中无明显现象,A中的现象是_____________、_______________。实验证明铁制品的锈蚀主要是铁与空气中的________________共同作用的结果。
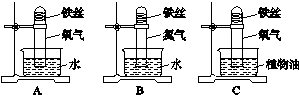
图Z3-27
(2)铁制品锈蚀可用稀硫酸除去铁锈,反应的化学方程式为_______________________________________________。
(3)2017年葫芦岛市投放了若干辆共享单车,制造这种单车使用了大量的铁合金,该合金与铁相比具有的优点是____________________。
(1)铁丝生锈 试管内液面上升 氧气和水蒸气
(2)Fe2O3+3H2SO4===Fe2(SO4)3+3H2O
(3)硬度大(或耐腐蚀)
1一些金属易生锈,某小组同学设计如下实验,对金属锈蚀进行探究。
[实验一] 取5枚去油去锈的洁净铁钉,分别装入下表的试管中,进行实验。
| 实验 图示 |
|
|
|
|
|
| 生锈 时间 | 8 min | 较长时间 不生锈 | 5 min | 3 min | 1 min |
(1)通过上述实验可知,温度越高,铁生锈速率越________(填“慢”或“快”);在__________(填“酸性”“碱性”或“中性”)环境中铁钉生锈速率较快。
[实验二] 为探究铁锈的成分,用如图Z3-28所示装置(夹持仪器已省略)进行实验(每步反应和吸收均完全)。
[查阅资料] 无水硫酸铜能吸收水而变蓝,碱石灰既能吸收水也能吸收CO2。
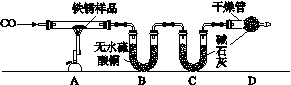
图Z3-28
(2)请指出上图所示实验装置的一个明显缺陷:______________________。
(3)加热前,先通入CO一段时间,目的是____________________________________。
(4)将铁锈样品加热,样品逐渐变黑,无水硫酸铜逐渐变蓝,由此推知铁锈中一定含有________元素,从而推断出空气中的________参加了铁生锈反应。
[实验记录]
| 铁锈样品的质量/g | 装置B的质量/g | 装置C的质量/g | |
| 反应前 | 23.2 | 232.4 | 198.2 |
| 反应后 | / | 239.6 | 211.4 |
(5)根据上表数据推算,可确定铁锈的成分,用FexOy·nH2O表示,则n=________;若缺少D装置,x∶y的值________(填“偏大”“偏小”或“无影响”)。
[实验三] 镁带久置空气中,表面因锈蚀而变黑,此黑色物质是碱式碳酸镁(带结晶水的碳酸镁和氢氧化镁的混合物)。
(6) 欲通过如图Z3-29所示装置探究镁带在空气中锈蚀的条件,试管内可选用的物质如下:①O2,②水,③CO2,④O2和CO2,⑤CO2和水,⑥O2和水,⑦O2、CO2和水。至少需要选用________(填序号),才能达到探究镁带锈蚀的条件。
![]()
图Z3-29
(7)请写出镁带在空气中锈蚀,生成碱式碳酸镁[Mg3(OH)2(CO3)2]的化学方程式:________________________________________________________________________。
(1)快 酸性 (2)没有尾气处理装置
(3)排尽玻璃管内的空气,防止爆炸
(4)氢(或H) 水 (5)4 偏小 (6)④⑤⑥⑦
(7)6Mg+4CO2+2H2O+3O2===2Mg3(OH)2(CO3)2
本卷还有15题,登录并加入会员即可免费使用哦~

该作品由: 用户泓塽分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。