科学家米拉德发明了对防治植物病菌有神奇功效的“波尔多液”。化学社团的同学参加劳动实践活动结束后,欲模拟配制波尔多液,请你参与他们的探究活动。
小强同学称量16.0g氧化铜粉末加入烧杯中,向烧杯中加入184.0g稀硫酸,用玻璃棒不断搅拌,烧杯中的黑色粉末逐渐溶解至消失,两者恰好完全反应,得到蓝色溶液。
(1)计算所得溶液溶质的质量分数。(写出计算过程)
(2)同学们查阅资料后得知,波尔多液是由硫酸铜、 和水按一定比例配制成的,它能够杀菌、防治植物病菌的原理是 。
(1)见解析
(2)生石灰 Cu2+能破坏病原体细胞膜从而影响其生物活性的原理
【分析】
(1)利用氧化铜能和稀硫酸反应,根据氧化铜的质量可以计算出所得溶液溶质的质量进而计算出溶液溶质的质量分数;
(2)根据“波尔多液”的配制原理和杀菌原理分析。
【解析】解:(1)设所得溶液中溶质的质量为x。
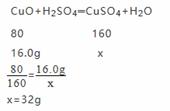
所得溶液溶质的质量分数=![]() ×100%=16%
×100%=16%
答:所得溶液溶质的质量分数16%;
(2)将硫酸铜、生石灰、水按一定比例混合,可以配制成农药“波尔多液”;硫酸铜中Cu2+能破坏病原体细胞膜从而影响其生物活性。
【点评】此题是对化学方程式计算以及重金属盐的杀菌原理的考查,解题的关键是能够对相关的反应情况进行的分析。
学习了金属矿物及其冶炼后,同学们设计了两组实验装置,请回答:
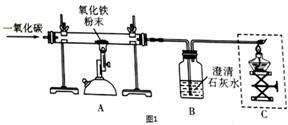
(1)铁元素在自然界中分布很广,氧化铁是 (填写铁矿石名称)的主要成分。如图1是用一氧化碳还原氧化铁粉末的实验装置,反应一段时间后,观察到玻璃管中的氧化铁粉末逐渐变成 色,装置B中的现象是 ,虚线框内装置的作用是 (填字母序号)。
a.吸收二氧化碳 b.消耗一氧化碳 c.检验一氧化碳
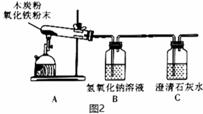
(2)如图2是用适量木炭粉还原氧化铁粉末的实验装置,写出反应的化学方程式: ,试管口部略向下倾斜的原因是 。反应一段时间后,装置C中澄清石灰水无现象的原因是 (用化学方程式表示)。
同学们发现一氧化碳和二氧化碳的组成元素相同,但性质有所不同。以下说法正确的是
(填字母序号)。
a.一氧化碳不能与水反应,二氧化碳能与水反应
b.一氧化碳和二氧化碳的分子结构不同
c.一氧化碳和二氧化碳都可以作气体肥料
d.一氧化碳和二氧化碳都可以作还原剂
(1)赤铁矿 黑 澄清的石灰水变浑浊 b
(2)3C+2Fe2O3![]() 4Fe+3CO2 防止冷凝水倒流、炸裂试管
4Fe+3CO2 防止冷凝水倒流、炸裂试管
2NaOH+CO2=Na2CO3+H2O ab
【分析】
(1)根据矿石的主要成分、一氧化碳的还原性、二氧化碳的性质以及处理尾气的方法来分析;
(2)根据化学反应的原理、固体加热的注意事项、氢氧化钠的性质、一氧化碳和二氧化碳的性质来分析。
【解析】解:(1)氧化铁是赤铁矿的主要成分;一氧化碳具有还原性,在高温的条件下,一氧化碳和氧化铁反应生成铁和二氧化碳,所以玻璃管中的氧化铁粉末逐渐变成黑色,二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,所以装置B中澄清的石灰水变浑浊;尾气中含有有毒的一氧化碳气体,为了防止排放到空气中造成污染,所以将尾气点燃处理;
(2)在高温的条件下,碳和氧化铁反应生成铁和二氧化碳,化学方程式为:3C+2Fe2O3![]() 4Fe+3CO2;给试管中的固体加热时,为防止冷凝水倒流、炸裂试管,所以试管口应略向下倾斜;装置B中的氢氧化钠溶液能与二氧化碳反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O,所以装置C中澄清石灰水无现象;
4Fe+3CO2;给试管中的固体加热时,为防止冷凝水倒流、炸裂试管,所以试管口应略向下倾斜;装置B中的氢氧化钠溶液能与二氧化碳反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O,所以装置C中澄清石灰水无现象;
a.一氧化碳不能与水反应,二氧化碳能与水反应,选项说法正确;
b.一氧化碳和二氧化碳的分子结构不同,选项说法正确;
c.一氧化碳不能作气体肥料,二氧化碳可以作气体肥料,选项说法错误;
d.一氧化碳具有还原性,可以作还原剂;二氧化碳没有还原性,不能用作还原剂,选项说法错误。
【点评】本题考查的是常见的物质的性质以及物质间的反应的知识,完成此题,可以依据已有的知识进行。
如图是实验室常用的部分实验装置,请回答下列问题。
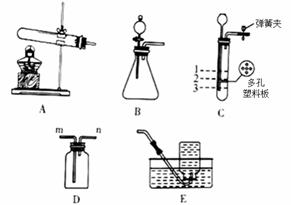
(1)用大理石和稀盐酸制取二氧化碳,反应的化学方程式是 。若用装置D收集二氧化碳,气体应从 (填“m”或“n”)端进入。若用装置C作发生装置,反应停止后,液面应位于 (填“1”、“2”或“3”)处。
(2)用过氧化氢溶液和二氧化锰粉末制取氧气,应选择的发生装置是 (填字母序号),写出反应的化学方程式: 。若用高锰酸钾制取氧气,应选择的发生装置是 (填字母序号)。用装置E收集氧气,当观察到 时,证明氧气收集已满。小红同学用此方法收集了一瓶氧气,测得氧气的纯度偏低,原因可能是 (填字母序号)。
a.收集气体前,集气瓶中没有注满水
b.导管口开始有气泡冒出,立刻收集
c.收集气体后,集气瓶中仍有少量水
d.收集气体后,集气瓶正放在桌面上
(1)2HCl+CaCO3=CaCl2+H2O+CO2↑ m 3
(2)B 2H2O22![]() H2O+O2↑ A 集气瓶口出现大气泡 ab
H2O+O2↑ A 集气瓶口出现大气泡 ab
【分析】(1)盐酸与碳酸钙反应生成氯化钙、水和二氧化碳,据此书写化学方程式;根据气体密度选择进气口;根据题目要求回答此题;
(2)根据反应物状态和反应条件选择发生装置;过氧化氢在二氧化锰催化作用下反应生成水和氧气,据此书写化学方程式;根据反应物状态和反应条件选择发生装置;根据排水法收集气体的注意事项回答此题;根据选项内容分析回答此题。
【解析】
解:(1)大理石主要成分碳酸钙,盐酸与碳酸钙反应生成氯化钙、水和二氧化碳,书写化学方程式注意配平及气体符号,所以化学方程式为2HCl+CaCO3=CaCl2+H2O+CO2↑;二氧化碳密度比空气大,先在底部聚集,应从m进气;反应停止后固液应该不接触,所以液面位于3处;
(2)反应物为固液混合物,二氧化锰为粉末,所以选择B为发生装置;过氧化氢在二氧化锰催化作用下反应生成水和氧气,书写化学方程式注意配平及气体符号,所以化学方程式为2H2O2![]() 2H2O+O2↑;反应物为固体且需要加热,所以选择A为发生装置;排水法收集气体时,瓶口出现大气泡,说明气体集满逸出,形成了气泡;
2H2O+O2↑;反应物为固体且需要加热,所以选择A为发生装置;排水法收集气体时,瓶口出现大气泡,说明气体集满逸出,形成了气泡;
a、集气瓶内未装满水,则内部混有空气,收集完毕后造成氧气纯度偏低,a符合题意;
b、导管口刚出现的气泡为内部受热膨胀逸出的空气,不能收集,若直接收集则进入氧气,造成氧气纯度偏低,b符合题意;
c、收集气体后,仍存有水,说明未集满,但是收集的氧气都是纯氧,不会造成纯度降低,c不符合题意;
d、氧气密度比空气大,在底部聚集,所以正放于桌面,不会引起纯度变化,d不符合题意,【点评】在解此类题时,首先要将题中的知识认知透,然后结合学过的知识进行解析。
兴趣小组的同学借助pH传感器监测溶液pH的变化情况来探究稀盐酸和氢氧化钠溶液的反应。如图1是反应装置和反应过程中溶液的pH变化曲线。
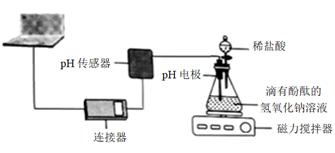

图1 图2
请据图回答:向锥形瓶中缓慢滴入稀盐酸,能说明稀盐酸与氢氧化钠溶液发生化学反应的现象是 ,写出反应的化学方程式: ,此反应类型属于 。当两者恰好完全反应时,溶液的pH位于曲线的 (填“m”、“n”或“f”)点。
下列说法是同学们在分析实验数据时得出的结论,你认为正确的是 (填字母序号)。
a.实验过程中氢氧化钠的质量不断变小直至为0
b.实验过程中使用磁力搅拌器的目的是吸收热量
c.实验过程中氯化钠的质量分数一直在不断增大
d.实验过程中也可以选用pH试纸验证反应的发生
溶液由红色变为无色 HCl+NaOH═NaCl+H2O 复分解反应 n a
【分析】根据滴有酚酞溶液的氢氧化钠溶液显红色,结合无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红,图象中pH值的变化是从大于7逐渐减小到小于7,进行分析解析。
【解析】
解:滴有酚酞溶液的氢氧化钠溶液显红色,无色酚酞溶液遇酸性溶液不变色,遇碱性溶液变红,逐滴滴入稀盐酸,至恰好完全反应,溶液显中性,溶液由红色变为无色,证明盐酸和氢氧化钠发生了化学反应。
稀盐酸与氢氧化钠反应生成氯化钠和水,反应的化学方程式为HCl+NaOH═NaCl+H2O。该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应。
当两者恰好完全反应时,溶液显中性,pH=7,则溶液的pH位于曲线的n点。
a.随着反应的进行,氢氧化钠被消耗,实验过程中氢氧化钠的质量不断变小直至为0,故选项说法正确。
b.实验过程中使用磁力搅拌器的目的是混匀反应物,确保充分反应,故选项说法错误。
c.实验过程中氯化钠的质量分数不是一直在不断增大,完全反应后,继续滴加稀盐酸,氯化钠的质量分数开始变小,故选项说法错误。
d.pH试纸上的标准比色卡上的数字只有整数,即使用pH试纸所测得的溶液酸碱度为整数,且使用pH试纸,需要多次进行检验,不好确定恰好完全反应的时机,实验过程中不能选用pH试纸验证反应的发生,故选项说法错误。
【点评】本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液pH大小之间的关系、从数形结合的角度理解中和反应是正确解析本题的关键.
小明同学要除去粗盐样品中的少量泥沙(已知:20℃时氯化钠的溶解度是36.0g),实验过程如图所示:
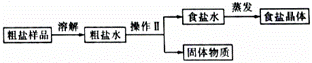
请回答:20℃时,小明要溶解10.0g粗盐样品,需量取 (填“15”、“30”或“45”)mL的水较为恰当,充分溶解后形成 (填“饱和”或“不饱和”)溶液,操作Ⅱ的名称是 。下列说法正确的是 (填字母序号)。
a.蒸发需要的仪器是酒精灯、蒸发皿、温度计
b.溶解和蒸发需要搅拌的目的是防止食盐飞溅
c.蒸发过程就是通过加热的方法将水汽化除去
30 不饱和 过滤 c
【分析】根据20℃时氯化钠的溶解度是36.0g,进行分析解析。根据操作Ⅱ是将泥沙与食盐水分离,进行分析解析。根据溶解、过滤、蒸发操作的方法、注意事项,进行分析判断。
【解析】
解:20℃时氯化钠的溶解度是36.0g,含义是20℃时,100g水中最多溶解36g氯化钠,溶液达到饱和状态,则20℃时,小明要溶解10.0g粗盐样品,需水的质量为100g×![]() ≈27.8g(合27.8mL),需量取30mL的水较为恰当,充分溶解后形成不饱和溶液。操作Ⅱ是将泥沙与食盐水分离,是过滤操作。
≈27.8g(合27.8mL),需量取30mL的水较为恰当,充分溶解后形成不饱和溶液。操作Ⅱ是将泥沙与食盐水分离,是过滤操作。
a.蒸发需要的仪器是酒精灯、蒸发皿、玻璃棒、铁架台,故选项说法错误。
b.溶解需要搅拌的目的是加快溶解速率;蒸发需要搅拌的目的是防止食盐飞溅;故选项说法错误。
c.蒸发过程就是通过加热的方法将水汽化除去,故选项说法正确。
【点评】本题难度不大,掌握粗盐提纯的原理、实验步骤(溶解、过滤、蒸发)、所需的仪器是正确解析本题的关键.
本卷还有17题,登录并加入会员即可免费使用哦~

该作品由: 用户墨_墨分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。