硼及其化合物在现代工农业、医学、国防中有着重要的应用价值。利用硼镁矿可制备硼,工艺流程如下图所示。请回答下列问题:
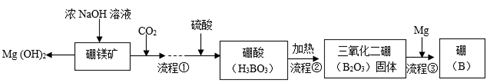
(1)B2O3中B元素的化合价为________。
(2)为加快硼镁矿石与浓NaOH溶液的反应速率,可采取的措施是_________;回收副产物Mg(OH)2可制得流程__________的反应物。
(3)H3BO3加热分解只生成两种氧化物,流程②的化学反应方程式为_________。
(4)根据流程③的化学反应方程式: ,理论上制备1.1吨的硼,需消耗镁多少吨写出计算过程)_________?
,理论上制备1.1吨的硼,需消耗镁多少吨写出计算过程)_________?
(1). +3 (2). 将硼镁矿石粉碎 (3). ③ (4). ![]() (5). 3.6t
(5). 3.6t
【解析】(1)氧元素通常显-2价,设B2O3中B元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:2x+(-2)×3=0,x=+3,故B元素的化合价为+3;
(2)为加快硼镁矿石与浓NaOH溶液的反应速率,可采取的措施是:将硼镁矿石粉碎,增大反应物之间的接触面积;
根据图中各反应的反应物,结合质量守恒定律,化学反应前后,元素的种类不变,氢氧化镁只可用于制取镁,故可制得流程③的反应物;
(3)H3BO3加热分解只生成两种氧化物,由图可知,H3BO3加热分解生成三氧化二硼,根据质量守恒定律,化学反应前后,元素的种类不变,反应物中含H、B、O,生成物中含B、O,故生成物中还应含H,故另一产物是水,流程②的化学反应方程式为![]() ;
;
(4)解:设理论上制备1.1吨的硼,需消耗镁的质量为x

![]() x=3.6t
x=3.6t
答:理论上制备1.1吨的硼,需消耗镁3.6吨。
酸碱中和反应是初中阶段重要的一类反应,请你一起参与探究。
【实验探究Ⅰ】在50mL一定浓度的氢氧化钠溶液中滴加50mL一定浓度的盐酸,并用玻璃棒搅拌,观察到溶液的温度______,由此现象小李同学得出两者能发生反应的结论。通过查阅相关资料后,小张同学发现此结论不够严谨,设计了下列3个对比实验:
①50mL一定浓度的盐酸与50mL蒸馏水混合,测量溶液温度的变化。
②50mL一定浓度![]() 氢氧化钠溶液与50mL蒸馏水混合,测量溶液温度的变化。
氢氧化钠溶液与50mL蒸馏水混合,测量溶液温度的变化。
③50mL一定浓度![]() 盐酸与50mL一定浓度的氢氧化钠溶液混合,测量溶液温度的变化。
盐酸与50mL一定浓度的氢氧化钠溶液混合,测量溶液温度的变化。
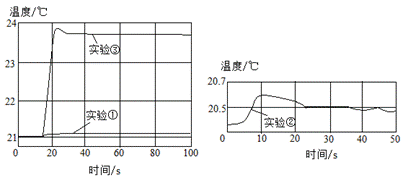
用数字化实验技术测得3个实验,溶液温度随时间变化的关系如图所示。
(1)由图可知,盐酸、氢氧化钠溶液稀释时均________(填“放热”或“吸热”),但它们稀释时温度的变化量远________两溶液混合时温度的变化量。
(2)从微观角度分析,此中和反应的温度变化主要是由于________(填离子符号)两种离子发生反应放出热量的缘故。
【实验探究Ⅱ】
(1)在50mL一定浓度的氢氧化钠溶液中滴加2~3滴酚酞试液,再逐滴加入一定浓度的盐酸,并用玻璃棒搅拌,溶液颜色由红色刚好变为无色时,可说明两者发生了反应。该反应的化学方程式为________。
(2)取一定量反应后的无色溶液加热蒸发,在蒸发的过程中,“意外”发现溶液由无色又变成红色。同学们对红色溶液中溶质的成分(酚酞除外)进行再探究。
查阅资料:酚酞在pH<8.2的溶液中呈无色,在8.2<pH<14的溶液中呈红色。
作出猜想:猜想一:NaCl
猜想二:NaCl、NaOH
猜想三:NaCl、NaOH和Na2CO3
同学们讨论后一致认为猜想__________是错误的,理由是___________。
实验验证:取样,滴加_______,无气泡产生,猜想三错误。
原因分析:反应后无色溶液中仍存在少量NaOH,加热蒸发,当溶液的pH在_______范围内,溶液的颜色变红。
总结反思:向某碱性溶液中滴加2~3滴无色酚酞试液,振荡后溶液的颜色_____(填“一定”或“不一定”)变红。
(1). 升高 (2). 放热 (3). 小于 (4). H+、OH- (5). ![]() (6). 三 (7). 反应物中不含碳元素 (8). 足量稀盐酸 (9). 8.2~14 (10). 不一定
(6). 三 (7). 反应物中不含碳元素 (8). 足量稀盐酸 (9). 8.2~14 (10). 不一定
【解析】(实验探究Ⅰ)在50mL一定浓度的氢氧化钠溶液中滴加50mL一定浓度的盐酸,并用玻璃棒搅拌,因中和反应放热,可观察到溶液的温度升高;
(1)由图可知,实验①、实验②中,溶液在稀释过程中温度都有上升,故盐酸、氢氧化钠溶液稀释时均放热,结合实验③曲线,可以发现盐酸、氢氧化钠溶液稀释时温度的变化量远低于两溶液混合时温度的变化量;
(2)从微观角度分析,此中和反应的温度变化主要是由于氢离子和氢氧根离子两种离子发生反应生成水分子放出热量的缘故,氢离子和氢氧根离子的离子符号分别是:H+、OH-。
(实验探究Ⅱ)
(1)在50mL一定浓度的氢氧化钠溶液中滴加2~3滴酚酞试液,再逐滴加入一定浓度的盐酸,并用玻璃棒搅拌,溶液颜色由红色刚好变为无色时,可说明两者发生了反应。氢氧化钠和盐酸反应生成氯化钠和水,该反应的化学方程式为:![]() ;
;
(2)根据质量守恒定律可知,反应前后元素种类不变,因此猜想三是错误的,理由是反应物中没有碳元素;
实验验证:取样,滴加足量的稀盐酸,无气泡产生,猜想三错误,因为碳酸钠能和盐酸反应生成二氧化碳气体,产生气泡;(本题中用足量的稀硫酸、稀硝酸均可)
原因分析:由资料可知,酚酞在pH<8.2的溶液中呈无色,在8.2<pH<14的溶液中呈红色。反应后无色溶液中仍存在少量NaOH,加热蒸发,随着溶剂水的不断减少,氢氧化钠的浓度逐渐增大,溶液的pH逐渐增大,当溶液的pH在8.2<pH<14范围内,溶液的颜色变红;
总结反思:根据资料,酚酞在pH<8.2的溶液中呈无色,如果碱性溶液的pH<8.2,滴加酚酞溶液,溶液的颜色就不会变红。因此向某碱性溶液中滴加2~3滴无色酚酞试液,振荡后溶液的颜色不一定变红。
请回答下列问题:
(1)现提供下列实验仪器和装置:
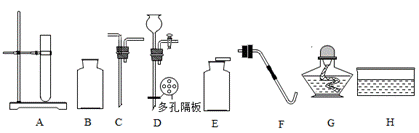
①实验室用高锰酸钾制氧气,反应的化学方程式为_______;该实验可选用F和____(填序号)组装成排水法收集氧气的装置;还可用_____方法收集氧气。
②实验室用锌粒和稀硫酸制氢气,反应的化学方程式为________;为达到控制反应生和停止的目的,发生装置应选择A和_____(填序号);为除去氢气中的水分,用B、C组装成一套装置,向B中加入液体试剂________,气体通过此装置达到目的。
(2)实验室用氯化钠固体配制50g溶质质量分数为15%的氯化钠溶液。
①量取水,应选择_________(填“10mL”或“50mL”)量筒。
②下列操作导致氯化钠溶液的溶质质量分数偏大的是_______(填序号)。
a.取用潮湿的氯化钠
b称量时,所用砝码表面已生锈
c量取水时仰视读数
d转移溶液后,烧杯内还有少量氯化钠固体
(1). ![]() (2). E、H (3). 向上排空气的 (4).
(2). E、H (3). 向上排空气的 (4). ![]() (5). D (6). 浓硫酸 (7). 50mL (8). b
(5). D (6). 浓硫酸 (7). 50mL (8). b
【解析】(1)①高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,该反应的化学方程式![]() ,该实验可选用E、F和H组装成排水法收集氧气的装置;
,该实验可选用E、F和H组装成排水法收集氧气的装置;
氧气的密度比空气大,还可用向上排空气法方法收集氧气,故填:![]() ;E、H;向上排空气。
;E、H;向上排空气。
②实验室用锌粒和稀硫酸制氢气,锌与稀硫酸反应生成硫酸亚铁和氢气,反应的化学方程式为 ![]() ;
;
为达到控制反应生和停止的目的,发生装置应选择A和 D,在装置中,固体药品放在多孔隔板上,液体药品从长颈漏斗中加入,反应开始后,关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行,装置的优点是可以随时控制反应的发生与停止;
为除去氢气中![]() 水分,用B、C组装成一套装置,浓硫酸具有吸水性,且不与氢气反应,向B中加入液体试剂浓硫酸,气体通过此装置达到目的,故填:
水分,用B、C组装成一套装置,浓硫酸具有吸水性,且不与氢气反应,向B中加入液体试剂浓硫酸,气体通过此装置达到目的,故填:![]() ;D;浓硫酸。
;D;浓硫酸。
(3)①实验室用氯化钠固体配制50g溶质质量分数为15%的氯化钠溶液,需水质量50g×(1-15%)=42.5g,体积![]() 量取水,应选择50mL量筒,故填:50mL。
量取水,应选择50mL量筒,故填:50mL。
② a.取用潮湿的氯化钠,氯化钠偏少,溶质质量分数偏小,不符合题意。
b称量时,所用砝码表面已生锈,称量药品偏多溶质质量分数偏大,符合题意。
c量取水时仰视读数,水偏多,溶质质量分数偏小,不符合题意。
d转移溶液后,烧杯内还有少量氯化钠固体,氯化钠没有全部溶解,溶质偏少,溶质质量分数偏小,不符合题意。
故选:b。
A~F是初中化学常见物质。A是生命之源,是人体中含量最多的物质;B与A发生化合反应生成C,C俗称熟石灰;D是由三种非金属元素组成的盐,D和A混合,溶液温度显著降低,据此原理可制作“摇摇冰”;C与D混合加热反应生成A、E、F三种物质,E为有刺激性气味的气体。请回答下列问题:
(1)A的化学式为________;电解A的实验,正、负极产生的气体体积比为________。
(2)B俗称_________,B与A反应的化学方程式为__________。
(3)C的澄清溶液通常用来检验__________气体。
(4)D在农业上可用作________________肥。
(5)E能使湿润的红色石蕊试纸变______________色。
(6)C与D混合加热反应的化学方程式为________。
(1). H2O (2). 1:2 (3). 生石灰 (4). ![]() (5). 二氧化碳(或 CO2) (6). 氮 (7). 蓝 (8).
(5). 二氧化碳(或 CO2) (6). 氮 (7). 蓝 (8). ![]()
【解析】(1)A~F是初中化学常见物质。A是生命之源,是人体中含量最多的物质;A的化学式为 H2O;电解A的实验,正、负极产生的气体体积比为1:2;
(2)B与A发生化合反应生成C,C俗称熟石灰;B是氧化钙,俗称 生石灰 ,B与A反应的化学方程式为CaO+ H2O= Ca(OH)2;
(3)二氧化碳能和氢氧化钙反应生成碳酸钙沉淀和水,氢氧化钙的澄清溶液通常用来检验二氧化碳气体;
(4)D是由三种非金属元素组成的盐,D和A混合,溶液温度显著降低,据此原理可制作“摇摇冰”,可知D是硝酸铵,在农业上可用作氮肥;
(5)C与D混合加热反应生成A、E、F三种物质,E为有刺激性气味的气体,可知E为氨气,氨气溶于水形成氨水,E能使湿润的红色石蕊试纸变蓝色;
(6)氢氧化钙与硝酸铵混合加热反应生成硝酸钙、氨气、水,化学方程式为![]() 。
。
在抗击新冠肺炎的过程中,测体温,戴口罩、勤消毒等是必需的防疫措施。
(1)水银体温计中的汞是由__________直接构成;测量体温,汞柱上升,汞微粒之间的___________增大。
(2)医用防护口罩使用了超细聚丙烯纤维,聚丙烯纤维属于___________材料;戴口罩能有效阻隔可吸入颗粒物、细菌、病毒等,其阻隔原理与化学实验中的__________基本操作类似。
(3)免洗手消毒液中含有的酒精,可使细菌中的蛋白质_____达到消毒目的;由于酒精具有_____性,开瓶用后应立即拧紧瓶盖,以免浓度降低;酒精使用时应远离火种,酒精不慎泼洒燃烧,灭火的方法是_____。
(1). 汞原子 (2). 空隙 (3). 合成 (4). 过滤 (5). 变性或失去生理活性 (6). 挥发 (7). 用湿抹布扑灭
【解析】(1)水银体温计中的汞是由汞原子直接构成;测量体温,汞柱上升,汞原子之间的间隔增大;
(2)医用防护口罩使用了超细聚丙烯纤维,聚丙烯纤维属于合成材料,是合成材料;戴口罩能有效阻隔可吸入颗粒物、细菌、病毒等,其阻隔原理与化学实验中的过滤基本操作类似,都是根据孔对颗粒大小不同的物质进行选择透过;
(3)免洗手消毒液中含有的酒精,可使细菌中的蛋白质变性或失去生理活性,达到消毒目的;由于酒精具有挥发性,开瓶用后应立即拧紧瓶盖,以免浓度降低;酒精使用时应远离火种,酒精不慎泼洒燃烧,灭火的方法是用湿抹布扑灭,原理是隔绝氧气。
本卷还有15题,登录并加入会员即可免费使用哦~

该作品由: 用户liven分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。