某种碳单质多孔材料中掺杂了氧化铁,为测定该材料中碳元素的含量,取 3.7g 样品进行实验,装置如下图所示。 ( 夹持仪器省略,空气中 CO 2 对实验的影响忽略不计 )
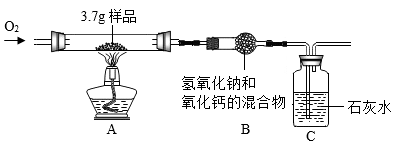
通入氧气,点燃酒精灯,使样品充分燃烧,一段时间后停止通氧气; C 中始终未出现浑浊。
(1) 氧化铁的化学式是 。
(2) 写出碳完全燃烧的化学方程式 。
(3) 将反应后装置 B 中药品放入水中搅拌,过滤。经检验,滤渣的成分是碳酸钙和氢氧化钙,其中碳酸钙的质量为 30.0g ;滤液中溶质的成分是 。
(4) 根据碳酸钙的质量能否确定样品中碳元素的含量,请分析说明 。
答案
(1)Fe 2 O 3
(2)
(3)NaOH 、 Ca(OH) 2
(4) 能,因为 C 中未出现浑浊,说明生成的 CO 2 全部转化为碳酸钙;根据碳元素质量守恒可知碳酸钙中碳元素的质量等于样品中碳元素的质量,从而确定样品中碳元素的含量
【详解】( 1 )氧化铁即三氧化二铁,其的化学式是 Fe 2 O 3 ;
( 2 )碳完全燃烧生成二氧化碳,其化学方程式为: ;
( 3 )某种碳单质多孔材料中掺杂了氧化铁,通入氧气,点燃酒精灯,使样品充分燃烧,完全反应后会产生二氧化碳,以及氧化铁(样品中原有的), B 装置吸收二氧化碳, B 装置内发生的反应有: 2NaOH+CO 2 =Na 2 CO 3 +H 2 O ; CaO+H 2 O=Ca(OH) 2 ; Ca(OH) 2 +Na 2 CO 3 =CaCO 3 ↓+2NaOH ;根据装置内存在的反应以及反应后装置 B 中药品放入水中搅拌、过滤,滤渣的成分是碳酸钙和氢氧化钙,说明溶液中不含有碳酸钠(碳酸钠会与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠),有 NaOH 、 Ca(OH) 2 ;
( 4 )根据碳酸钙的质量能确定样品中碳元素的含量,因为 C 中始终未出现浑浊,说明生成的 CO 2 在 B 中被全部吸收,即生成的二氧化碳全部转化为碳酸钙,根据碳元素质量守恒可知碳酸钙中碳元素的质量等于样品中碳元素的质量,从而确定样品中碳元素的质量。