催化剂可显著提高反应效率,二氧化锰是常见的催化剂。
(1) 实验室用 H 2 O 2 溶液制取氧气,常用 MnO 2 作催化剂反应的化学方程式是 ;用排水法收集氧气,是因为氧气 ( 选填 “ 易 ” 或 “ 不易 ”) 溶于水;将带火星的木条伸入盛有氧气的集气瓶中,现象是 。
(2)FeCl 3 对 H 2 O 2 分解也有催化作用。为比较 MnO 2 和 FeCl 3 对 H 2 O 2 分解快慢的不同影响,用下图左装置进行实验:启动传感器,注入 H 2 O 2 溶液。氧气体积分数随时间变化情况如下:
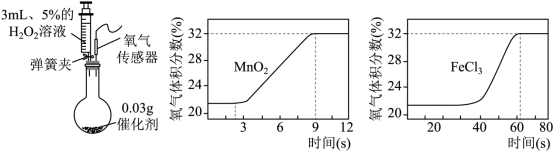
i. 初始时氧气的体积分数不为 0 ,原因是 。
ii. 写出使 H 2 O 2 分解较快的催化剂及判断依据: 。
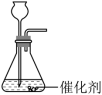
iii. 用 5% H 2 O 2 溶液制取氧气,若采用下图所示装置进行实验,上述两种催化剂中较为合适的是 。
答案
(1) 不易 带火星木条复燃
(2) 装置中含有空气,空气中约含 21% 体积的氧气 MnO 2 , 因为 MnO 2 作催化剂时,产生等量氧气所需的时间比 FeCl 3 短 FeCl 3
【详解】( 1 ) ① 实验室用 H 2 O 2 溶液制取氧气的原理是:过氧化氢在二氧化锰催化剂条件下分解生成水和氧气,该反应的化学方程式为: ,故填:
。
② 由于氧气不易溶于水,可用排水法收集,故填:不易。
③ 氧气具有助燃性,能使带火星木条复燃,所以将带火星的木条伸入盛有氧气的集气瓶中,观察到的现象是带火星木条复燃,故填:带火星木条复燃。
( 2 ) ① 由于装置中空气含有氧气,氧气约占空气体积的 21% ,所以初始时氧气的体积分数不为 0 ,故填:装置中含有空气,空气中约含 21% 体积的氧气。
② 比较 MnO 2 和 FeCl 3 使 H 2 O 2 分解快慢的曲线图,可知当氧气体积分数都达到 32% 时,加 MnO 2 用的时间为 9s ,加 FeCl 3 的时间大于 60s ;所以使 H 2 O 2 分解较快的催化剂是 MnO 2 ,原因是 MnO 2 作催化剂时,产生等量氧气所需的时间比 FeCl 3 短,故填: MnO 2 ,因为 MnO 2 作催化剂时,产生等量氧气所需的时间比 FeCl 3 短。
③ 选择 FeCl 3 可以使 H 2 O 2 分解反应速率适中,得到平稳的氧气流,故填: FeCl 3 。