如图所示是甲、乙、丙三种物质 ( 均不含结晶水 ) 的溶解度曲线,请据图判断下列说法中错误的是
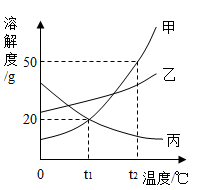
A .要从甲物质饱和溶液中获取晶体甲,可采用降温结晶的方法
B . t 2 ℃ 时,将 30g 甲物质加入到 50g 水中充分溶解后可以形成 80 克溶液
C .要配制相同质量分数的甲、丙两种物质的饱和溶液,应将温度控制 t 1 ℃
D . t 1 ℃ 时,甲、乙、丙三种物质的溶解度大小关系为:乙 > 甲 = 丙
答案
B
【详解】 A 、如图所示,甲的溶解度受温度影响大,因此要从甲物质饱和溶液中获取晶体甲,可采用降温结晶的方法,选项正确;
B 、 t 2 ℃ 时,甲的溶解度是 30g ,说明该温度下 100g 水中最多溶解饱和 30g 甲,则将 30g 甲物质加入到 50g 水中充分溶解后会有 15g 甲未溶解,可以形成 65g 溶液,选项错误;
C 、要配制相同质量分数的甲、丙两种物质的饱和溶液,说明此时两物质的溶解度相等,根据图像 t 1 ℃ 时甲和丙的溶解度曲线交于一点,此时溶解度相等,故应将温度控制 t 1 ℃ ,选项正确;
D 、 t 1 ℃ 时,甲、乙、丙三种物质的溶解度点,乙在最上面,甲和丙重合,则大小关系为:乙 > 甲 = 丙,选项正确;
故选: B 。