甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答下列问题:
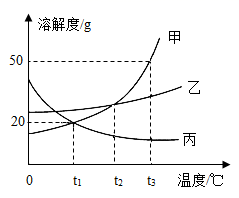
( 1 ) t 2 ℃时,甲、乙、丙三种物质溶解度的大小关系是 ________ (用 “>”、“<”或“=”表示)。
( 2 ) t 3 ℃时,甲物质的饱和溶液中溶质与溶剂的质量比为 ________ (填最简比)。
( 3 ) 甲中混有少量的乙,提纯甲的方法是 ________ 。
( 4 ) 将 t 3 ℃时甲、乙、丙三种物质的饱和溶液分别降温到 t 1 ℃,所得溶液中溶质的质量分数大小关系是 ________ (用 “>”、“<”或“=”表示)。
答案
( 1 ) 甲=乙>丙
( 2 ) 1 : 2
( 3 ) 降温结晶
( 4 ) 乙>甲>丙
【分析】
( 1 )
通过分析溶解度曲线可知, t 2 ℃ 时,甲、乙、丙三种物质溶解度的大小关系是甲=乙>丙;
( 2 )
t 3 ℃ 时,甲物质的溶解度是 50g ,所以甲物质的饱和溶液中溶质与溶剂的质量比为 50g : 100g = 1 : 2 ;
( 3 )
甲物质的溶解度受温度变化影响较大,乙物质溶解度受温度变化影响较小,所以甲中混有少量的乙,提纯甲的方法是降温结晶;
( 4 )
t1℃ 时,乙物质的溶解度最大,甲、丙物质的溶解度相等,将 t3℃ 时甲、乙、丙三种物质的饱和溶液分别降温到 t1℃ ,甲、乙物质的溶解度减小,析出晶体,丙物质的溶解度增大,不会析出晶体,丙的质量分数不变,所以所得溶液中溶质的质量分数大小关系是乙>甲>丙。