因发现青蒿素而获诺贝尔奖的科学家屠呦呦还发现了双青蒿素。查阅资料可知,双青蒿素由碳、氢、氧三种元素组成。为测定双青蒿素中碳、氢、氧三种元素的质量比,兴趣小组进行了以下探究。
(设计实验)兴趣小组设计并进行了如下图一所示的实验。(装置气密性良好)
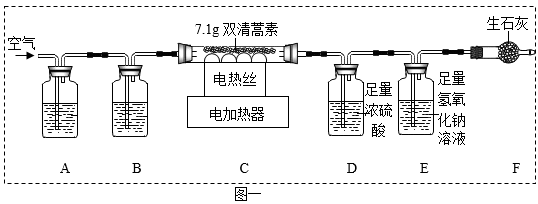
将 7.1g 双青蒿素放在装置 C 的玻璃管中,燃烧至无固体灰分残留。
( 1 )装置 A 、 B 中盛放的试剂分别是 ______ (填序号)。
①足量 NaOH 溶液、足量浓硫酸 ②足量浓硫酸、足量 NaOH 溶液
( 2 )装置 F 可吸收从装置 E 的气流中带出来的少量水蒸气,生石灰与水蒸气发生反应的化学方程式是 ______ 。
(记录数据)加热前,先通入空气一段时间,再称量装置 D 的质量、装置 E 和 F 的总质量(反应前的质量)。双青蒿素完全反应后,停止加热,继续通入空气一段时间,再次称量装置 D 的质量、装置 E 和 F 的总质量(反应后的质量)。实验数据如右表所示。
| 装置 | 反应前的质量 /g | 反应后的质量 /g |
| D | 74.7 | 80.1 |
| E 和 F | 80.3 | 96.8 |
(实验结论)( 3 )根据表中数据分析,双青蒿素中碳、氢、氧三种元素的质量比是 ______ 。
(拓展分析)( 4 )双青蒿素分子中碳、氢、氧三种原子的个数比是 ______ 。
(实验反思)( 5 )实验过程中加热前要先通入空气一段时间,该操作的作用是 ______ 。
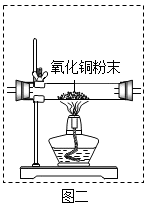
( 6 )有同学建议,为使实验结果更准确,需要在装置 C 和 D 之间增加图二所示的装置,其目的是 ______ 。
答案
① 45:6:20
排除装置中空气含有二氧化碳和水蒸气的干扰 将青蒿素不充分燃烧生成一氧化碳进行转化,减少实验误差
【详解】
( 1 )空气中含有二氧化碳和水蒸气,会干扰实验结果的测定;故装置 A 、 B 需要除去两者,氢氧化钠溶液可以吸收二氧化碳、浓硫酸可以吸收水,且气体应该先除杂后干燥防止气体带出氢氧化钠溶液中的水,故装置 A 、 B 盛放的试剂分别是 ①足量 NaOH 溶液、足量浓硫酸,选 ①。
( 2 )氧化钙和水反应生成氢氧化钙, 。
( 3 )装置 D 中浓硫酸吸收生成的水,装置增加质量就是生成水的质量 80.1-74.7=5.4g ;装置 E、F 可以吸收生成的二氧化碳气体及从装置 E 的气流中带出来的少量水蒸气,装置 E 和 F 的总质量增加就是生成二氧化碳的质量 96.8-80.3=16.5g ;反应前后元素种类质量不变,双青蒿素中碳、氢质量等于生成二氧化碳、水中碳、氢元素质量,分别为 、
,则 7.1g 双青蒿素中氧元素质量为 7.1-4.5-0.6=2g ,故双青蒿素中碳、氢、氧三种元素的质量比是 4.5g : 0.6g : 2g=45:6:20 。
( 4 )由( 3 )分析可知,双青蒿素分子中碳、氢、氧三种原子的个数比是 。
( 5 )开始前装置中的空气含有二氧化碳和水蒸气,会感染实验结果,实验过程中加热前要先通入空气一段时间,该操作的作用是排除装置中空气含有二氧化碳和水蒸气的干扰。
( 6 )如果双青蒿素不充分燃烧生成一氧化碳,不能被装置 EF 吸收造成实验误差,一氧化碳能还原氧化铜转化为二氧化碳被氢氧化钠溶液吸收,故为使实验结果更准确,需要在装置 C 和 D 之间增加图二所示的装置。



 五氧化二磷
五氧化二磷