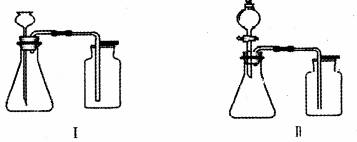某研究小组对过氧化氢溶液制取氧气进行如下探究 :
实验一 : 氧气制取和性质实验
(1) 现有如下装置
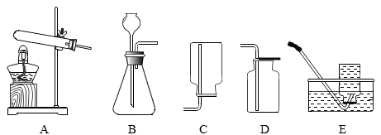
①实验室用过氧化氢溶液制氧气的化学方程式为 ______________________ , 应选择的发生装置和收集装置分别是 ____________ ( 填标号 , 下同 ) 和 ____________ 。
②检查 B 装置气密性的操作是 _____________________________ 。
③用收集的氧气进行 “ 铁丝在氧气中燃烧 ” 的实验 , 观察到的现象是 _______________ , 反应的化学方程式为 _______________________ 。
实验二 : 探究 H 2 O 2 质量分数、溶液 pH 、温度对反应速率的影响
(2) 设计如下表实验方案 :
| 实验序号 | H 2 O 2 质量分数 /% | pH | 温度 / ℃ | 每分钟气泡数 |
| 1 | 30 | 5 | 20 | |
| 2 | 30 | 6 | 20 | |
| 3 | 30 | 11 | 20 | |
| 4 | 15 | 11 | 30 | |
| 5 | a | 11 | b | |
①实验 1~3 的实验目的是 _____________________ 。
② a= ____________ ; b= ___________ 。
实验三:探究制取氧气的适宜催化剂
(3) 实验方案如下 :
I. 用 MnO 2 、 CuO、Fe 2 O 3 、 Cr 2 O 3 四种催化剂分别与海藻酸钠溶液混合 , 滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球 , 备用。
II. 取 30 粒含 MnO 2 的海藻酸钠微球 , 采用左下图装置进行实验。改用其他三种微球 , 分别重复上述实验 , 得到右下图的锥形瓶内压强随时间变化的曲线图。
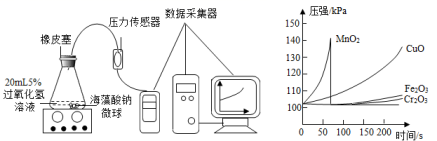
①每次实验时 , 海藻酸钠微球数应相同的原因 ________________________________ 。
②用含 MnO 2 的海藻酸钠微球进行实验 , 60s 时压强瞬间回落 , 其原因是 ____________ 。
③从实验曲线看 , 催化效果较好、反应温和的催化剂是 ___________________ 。
答案
2H 2 O 2 MnO 2 2H 2 O+O 2 ↑ B D 或 E 用止水夹夹住橡胶管,往长颈漏斗中加水形成一段水柱,观察水柱是否变化(或其他合理答案) 火星四射,生成一种黑色固体 3Fe+2O 2 点燃 Fe 3 O 4 探究溶液的 pH 对反应速率的影响 a=15,b=20 或 a=30,b=30 确保催化剂用量一致 产气速率过快,导致气压过大,橡胶塞被弹出(或其他合理答案) CuO
【解析】
(1) ①根据过氧化氢在二氧化锰的催化下分解生成水和氧气解答;根据反应物的状态、反应条件和生成氧气的密度和溶解性解答;②根据用止水夹夹住橡胶管,往长颈漏斗中加水形成一段水柱,观察水中柱是否变化解答;③根据铁在氧气中剧烈燃烧,火星四射,生成一种黑色固体解答; (2) 根据控制变量法分析解答; (3) ①根据确保催化剂用量一致解答;②根据压强瞬间回落可能是装置内压强与外界压强趋于一致分析解答;③根据实验曲线分析解答。 (1) ①过氧化氢在二氧化锰的催化下分解生成水和氧气,反应的化学方程式为 2H 2 O 2 MnO 2 2H 2 O+O 2 ↑ ;反应物是固体和液体混合,反应在常温下进行,故应选择的发生装置是 B ;由于氧气的密度比空气大不易溶于水,可以选择向上排空气法或排水法收集,可选择的收集装置是 D 或 E; ②检查 B 装置气密性的操作是用止水夹夹住橡胶管,往长颈漏斗中加水形成一段水柱,观察水柱是否变化; ③用收集的氧气进行“铁丝在氧气中燃烧”的实验,观察到的现象是火星四射,生成一种黑色固体,反应的化学方程式为 3Fe+2O 2 点燃 Fe 3 O 4 ; (2) ①由表中数据可知,过氧化氢溶液的质量分数相同,反应温度相同,溶液的pH不同,故实验 1~3 的实验目的是探究溶液的 pH 对反应速率的影响; ②对比分析实验 4、5 ,若控制的变量为温度,则 a=15,b=20 ;(或若控制的变量为 H 2 O 2 质量分数则 a=30,b=30 ) ; (3) ①每次实验时,海藻酸钠微球数应相同的原因是确保催化剂用量一致;②用含 MnO 2 的海藻酸钠微球进行实验, 60s 时压强瞬间回落,其原因是产气速率过快,导致气压过大,橡胶塞被弹出; ③从实验曲线看,催化效果较好、反应温和的催化剂是 CuO。

 K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑
 2H2O+O2↑
2H2O+O2↑