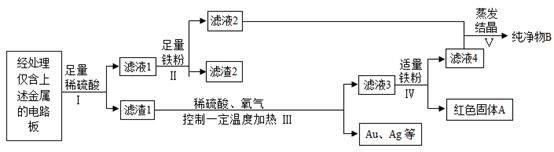
我国每年报废的手机超过1亿部。废旧手机的电路板中含有多种金属,随意丢弃会造成资源浪费并污染土壤和水体。某手机电路板中含有Sn、Fe、Cu、Au、Ag等金属,如图是某工厂回收其中部分金属的流程图。(其中Sn、Au在化合物中的化合价分别为+2价、+3价)
(1)过程Ⅰ、Ⅱ、Ⅳ均涉及的操作是_____,该操作需要用到一种金属材料制成的仪器是_____,需要用到的玻璃仪器有玻璃棒、烧杯和_____。
(2)写出过程Ⅱ中反应的化学方程式_____、_____。
(3)写出过程Ⅲ中反应的化学方程式_____。
(4)滤液4的主要成分(水除外)是_____。
答案
过滤 铁架台 漏斗 ![]()
![]()
![]() 硫酸亚铁
硫酸亚铁
【详解】
(1)由图可知,过程Ⅰ、Ⅱ、Ⅳ均是将固体与液体进行分离,涉及的操作为过滤,故填过滤,过滤操作中要用到的金属材料制成的仪器是铁架台,需要用到的玻璃仪器有玻璃棒、烧杯和漏斗;
(2)加入稀硫酸后,Sn和Fe能溶解于稀硫酸,而Cu、Au和Ag不能溶解于稀硫酸,成为滤渣,滤液Ⅰ中含有的主要成分为硫酸铜和硫酸锡,因为铁的活动性要强于铜和锡,因此铁能和硫酸锡发生置换反应,同时还发生了铁和硫酸的反应,反应方程式为![]() ,
, ![]()
(3)滤渣Ⅰ中有Cu、Au和Ag,铜能够和稀硫酸、氧气,在加热条件下反应生成硫酸铜。反应方程式为![]() ;
;
(4)根据图示可知滤液4的主要成分和滤液2的主要成分一致,滤液2主要成分为硫酸亚铁,故滤液4的主要成分是硫酸亚铁。

 Cu+H2O
Cu+H2O 2Fe+3H2O
2Fe+3H2O 2Cu+CO2↑
2Cu+CO2↑ 4Fe+3CO2↑
4Fe+3CO2↑