人类的生产、生活都离不开金属。
(1)人体中含量最高的金属元素是_____(填元素符号)。
(2)目前已制得的纯金属只有_____余种,日常生活中使用的金属或金属材料,大多数为合金。生铁和钢是两种含碳量不同的铁合金。钢的含碳量_____生铁的含碳量(填“大于”或“等于”或“小于”)。
(3)下列各组药品,可用于验证锌、铁、铜三种金属活动性顺序的是_____(填字母序号)。
A.Zn、Cu、FeSO4溶液 B.Fe、Cu、ZnSO4溶液
C.Fe、ZnSO4溶液、CuSO4溶液 D.Cu、ZnSO4溶液、FeSO4溶液
(4)向硝酸银和硝酸铜的混合溶液中加入一些锌粉,充分反应后过滤。若向滤渣中滴加稀盐酸没有气泡产生,则滤渣中一定含有的金属是_____,滤液中一定含有的溶质是_____。
(5)某种铁的氧化物6.96g在高温下与足量的一氧化碳充分反应,只生成二氧化碳和铁,其中二氧化碳为5.28g,经计算这种铁的氧化物为_____(填化学式)。
答案
Ca;90,小于;AC;Ag,硝酸锌;Fe3O4。
【解析】
(1)人体中含量最高的金属元素是Ca,主要存在与骨骼和牙齿中。(2)目前已制得的纯金属只有90余种。生铁和钢是两种含碳量不同的铁合金。钢的含碳量为0.03%~2%,生铁的含碳量为2%~4.3%。(3)金属活动性顺序中,排在前面的金属能把排在后面的金属从其化合物的水溶液中置换出来。A.Zn能与FeSO4溶液反应,证明 Zn>Fe,Cu不与FeSO4溶液反应,证明Fe>Cu,即Zn>Fe>Cu,此选项正确;B.Fe、Cu都不与ZnSO4溶液反应,证明三种金属中,Zn的金属活动性最强,不能证明Fe、Cu的金属活动性,此选项错误;C.Fe不与ZnSO4溶液反应,证明Zn>Fe,Fe能与CuSO4溶液反应,证明Fe>Cu,即Zn>Fe>Cu,此选项正确;D.Cu不能与ZnSO4溶液、FeSO4溶液反应,证明证明三种金属中,Cu的金属活动性最弱,不能证明Zn、Fe的金属活动性,此选项错误。故选AC。(4)金属活动性顺序中,排在前面的金属能把排在后面的金属从其化合物的水溶液中置换出来,且金属活动性差距越大,越易进行。向硝酸银和硝酸铜的混合溶液中加入一些锌粉,锌先与硝酸银溶液反应,Zn+2AgNO3==2Ag+Zn(NO3)2,当硝酸银溶液反应完以后,锌才与硝酸铜溶液反应, Zn +Cu(NO3)2 ==Cu+ Zn(NO3)2 ,充分反应后过滤,若向滤渣中滴加稀盐酸没有气泡产生,说明滤渣中无锌,锌发生了反应,则反应Zn+2AgNO3==2Ag+Zn(NO3)2肯定发生,所以滤渣中一定含有的金属是Ag,滤液中一定含有的溶质是Zn(NO3)2。(5)设该铁的氧化物的化学式是FexOy。
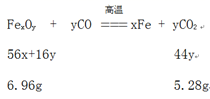
![]() =
=![]() ,解得
,解得![]() =
=![]() ,所以该铁的氧化物的化学式是Fe3O4
,所以该铁的氧化物的化学式是Fe3O4
【点睛】
在金属活动性顺序中,排在前面的金属能把排在后面的金属从其化合物的水溶液中置换出来,且金属活动性差距越大,越易进行。化学反应前后各种原子个数相等。
