
某化学小组在复习所学知识,提出这样的问题:实验室用过氧化氢溶液制取氧气时,用二氧化锰作催化剂,那么氧化铜是否也能作过氧化氢分解的催化剂呢?
(制订计划)要想知道氧化铜能否作过氧化氢分解的催化剂,必须通过实验确定。
(1)氧化铜能否改变过氧化氢分解的速率;
(2)研究氧化铜在过氧化氢分解反应前后____________和____________是否改变。
(进行实验)(1)在两支试管中分别加入过氧化氢溶液,在其中一支试管中加入1g氧化铜粉末,比较反应速率。现象是:_________________。
(2)从反应后的物质中分离固体剩余物,把固体干燥后称量,其质量为1g。
(3)利用上一步中得到的固体,重复做前两步实验,得到相同的结果。
(得出结论)氧化铜能作过氧化氢分解的催化剂。
(反思总结)实验过程中加入到两支试管里的过氧化氢溶液应满足的要求有:_________。
①体积相同 ②浓度相同 ③温度相同
质量 化学性质 加氧化铜粉末的试管比不加氧化铜的试管产生气泡快 ①②③
【详解】
(制订计划)催化剂是在化学反应里能改变其他物质的化学反应速率(既能提高也能降低),而本身的质量和化学性质在化学反应前后都没有发生改变的物质;要想证明氧化铜是过氧化氢分解的催化剂就要证明氧化铜能否改变过氧化氢分解的速率,还要研究氧化铜在过氧化氢分解反应前后质量和化学性质有没有改变;
故答案为:质量;化学性质;
(进行实验)由于结论中氧化铜是过氧化氢分解的催化剂,所以可以加快过氧化氢的分解,所以加氧化铜粉末的试管比不加氧化铜的试管产生气泡快;
故答案为:加氧化铜粉末的试管比不加氧化铜的试管产生气泡快;
(反思总结)过氧化氢溶液分解产生的氧气时受①体积②浓度③温度的影响,所以要想证明氧化铜是催化剂就要控制其上述三个量相同,只改变氧化铜一个量;故答案为:①②③。

| 探究过程要素 | 达到目的 |
| 提出问题 | a.能从日常现象或化学学习中,经过启发或独立地发现一些有价值的问题 b.能比较清楚地表述所发现的问题 |
| 猜想与假设 | a.能主动地或在他人的启发下对问题可能的答案作出猜想或假设 b.具有依据已有的知识和经验对猜想或假设作出初步论证的能力 |
| 制订计划 | a.在教师指导下或通过小组讨论,提出活动方案,经历制定科学活动计划的过程 b.能在教师指导下或通过小组讨论,根据所要探究的具体问题设计简单的化学实验方案,并且具有控制实验条件的能力 |
| 进行实验 | a.能积极参与化学实验 b.能顺利地完成实验操作 c.能在实验操作中做到观察和思考相结合 |
| 收集证据 | a.具有较强的实证意识 b.学习运用各种方式对物质及其变化进行观察 c.能独立地或与他人合作对观察和测量的结果进行记录,并运用图表等形式加以表述 d.初步学会运用调查、资料查阅等方式收集解决问题所需要的证据 |
| 解释与结论 | a.能对事实与证据进行简单的加工与整理,初步判断事实与假设之间的关系 b.能依据一定的标准对物质及其变化进行简单的分类 c.能在教师的指导下或通过与他人讨论对所获得的事实与证据进行归纳,从而得出正确的结论 d.初步学会通过比较、分类、归纳、概括等方法认识知识之间的联系,形成合理的知识结构 |
| 反思与评价 | a.具有对探究结果的可靠性进行评价的能力 b.能在教师的指导下或通过与他人讨论,对探究学习活动进行反思,发现自己与他人的长处以及存在的不足,并提出改进的具体建议 c.能体验到探究学习活动的乐趣和成功的喜悦 |
| 表达与交流 | a.能用口头、书面等方式比较明确地表述探究过程和结果,并能与他人进行交流和讨论 b.与他人交流讨论时,既敢于发表自己的观点,又要善于倾听别人的意见 |
登录并加入会员可无限制查看知识点解析
下列实验方案与实验结论相对应的是( )
| 选 项 | A | B | C | D |
| 方 案 |
|
|
|
|
| 结 论 | 比较呼出气体中二氧化碳含量较空气中的多 | 说明白烟的成分与蜡烛成分相同 | 说明酒精灯火焰分为三层,而焰心温度最高 | 说明液态水与气态水可以相互转化 |
A.A B.B C.C D.D
维生素C是生命活动中不可缺少的营养物质,不同的饮料中维生素C的含量不同。下面是小明同学运用学到的实验方法测定橙汁、果味饮料中维生素C的含量。
《实验目的》测定不同饮料中维生素C的含量。
《实验原理》
(1)维生素C是一种无色易溶于水的有机物,能与碘水反应,使碘水褪色;
(2)淀粉遇到碘水变__________色。
《实验试剂》碘水、淀粉溶液、已知浓度的标准维生素C溶液、蒸馏水
《实验过程》
步骤1:在4支试管中分别盛有3.0 mL的下列物质:①蒸馏水,②标准维生素C溶液,
③橙汁,④果味饮料。分别向4支试管中滴加2滴淀粉溶液。
步骤2:用4支相同的胶头滴管分别向①~④支试管中逐滴滴加碘水至刚好变色,并记录滴数。
《实验记录》
| 测定物质 | ① | ② | ③ | ④ |
| 滴入碘水的数量(滴) | 1 | 8 | 15 | 5 |
试回答下列问题:
(1)你认为小明测定的两种饮料中, ____________________的维生素C的含量较高;
(2)有的同学认为测定物质标准维生素C溶液是多余的,你认为呢?请说明理由:________________________________________________________________________________________;
(3)化学实验需要控制变量。下列 ______________(填序号)情况会影响到测定结果。
A.每次实验所用饮料的颜色不同 B.量取的被测试物质的体积不同
C.试管的大小不同 D.没有用同一规格的胶头滴管滴加碘水
《回顾与反思》实验中所用的淀粉溶液的作用是________________________________。
学习氢氧化钠的性质之后,知道氢氧化钠溶液中含有H2O、Na+、OH-,能使无色酚酞溶液变红色,某科技小组想进一步探究是哪一种粒子使无色酚酞溶液变红色。
(提出猜想)猜想①:可能是H2O;
猜想②:可能是Na+;
猜想③:可能是OH-。
(实验验证)
| 实验操作 | 实验现象 | 结 论 |
| ①用试管取少量蒸馏水,滴入1滴~2滴无色酚酞溶液,振荡 | 试管内溶液仍为无色 | 水分子不能使无色酚酞溶液变红色 |
| ②用试管取少量氯化钠溶液,滴入1滴~2滴无色酚酞溶液,振荡 |
|
|
| ③用试管取少量氢氧化钠溶液,滴入1滴~2滴无色酚酞溶液,振荡 |
|
|
(讨论反思)有同学认为猜想①不需要实验验证就可以排除,你认为该同学的理由是__________________________。
在日常生活中,我们发现切过咸菜的刀更容易生锈.而除锈用稀盐酸比稀硫酸快。为了进一步验证上述现象,某校师生做了以下相关分组实验,请你根据自己平时课堂学习的体验一起参与讨论并回答相关问题。
(步骤一)未打磨的铝片浸入氯化铜溶液中,迅速产生大量气泡和疏松的紫红色固体,并放热,片刻后溶液由蓝绿色变成无色。
(1)若要正视紫红色固体中是否含有氧化铜,可用_______溶液(填一试剂)加以检验。
(步骤二)未打磨的铝片浸入硫酸铜溶液中,一段时间内没有明显现象。
(2)比较步骤一、二,你能得出的结论是:____________。
(步骤三)打磨过的铝片浸入硫酸铜溶液中,其操作、现象和结论见下表。
(3)试将“影响因素”选项前恰当的字母序号填入答题卡指定位置。
| 实验操作 | 使用现象 | 对比结论 |
| Ⅰ.一片用粗砂纸单向用力打磨3次,将其浸入硫酸铜溶液,片刻后用镊子取出。 | 现象一:粗砂纸打磨的在划痕处有少量气泡,附着少量疏松的紫红色固体。 | 现象一与现象二对比,说明 |
| 现象二:粗砂纸打磨的片刻内现象不明显。 | ||
| Ⅱ.一片用特细砂纸往复打磨数次,再将其浸入硫酸铜溶液,片刻后取出。 | 现象三:特细砂纸打磨的表面产生较多细小气泡,表面均匀附着紫红色固体。 | 现象三与现象一对比,说明 |
| 现象四:特细砂纸打磨的表面一段时间内没有明显现象。 | 现象四与现象三对比,说明 |
影响因素:
A打磨时用力程度及均匀程度不同
B选用砂纸颗粒粗细程度不同
C由于摩擦生热又形成了新的氧化膜
(4)比较步骤三各实验操作中用砂纸打磨的作用是:____________________。
(5)请仔细观察下图:
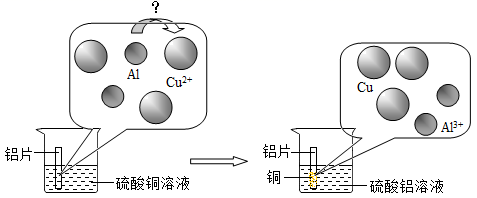
试从微观粒子变化的角度分析该反应的实质是:____________________。