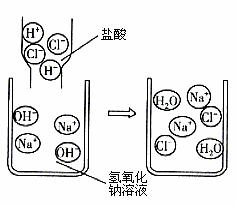
(2019·绥化)酸、碱、盐在生产生活中有着广泛的应用。
(1)氢氧化钠溶液与稀硫酸反应时,溶液pH变化如图11-4所示。
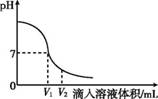
图11-4
①根据图示判断该实验是将 滴入到 中。
②滴入溶液体积为V2 mL时,溶液中溶质为 (填化学式)。此时滴入石蕊溶液的现象为 。
(2)测定某酸溶液pH时,如果放pH试纸的玻璃片上的水没有擦干就进行测定,会使测得的pH (填“偏大”或“偏小”)。
(3)用来改良酸性土壤的碱是 。
答案
(1)①稀硫酸 氢氧化钠溶液
②H2SO4、Na2SO4 石蕊溶液变红
(2)偏大
(3)熟石灰(或氢氧化钙或消石灰)
(解析) (1)①开始时溶液的pH大于7,故开始为碱性溶液,因此是将稀硫酸滴入到氢氧化钠溶液中;②滴入溶液体积为V2 mL时,稀硫酸过量,故溶液中溶质为生成的硫酸钠和剩余的硫酸,能使石蕊溶液变红。(2)酸溶液的酸性越弱,pH越大,测定某酸溶液pH时,如果放pH试纸的玻璃片上的水没有擦干就进行测定,会使酸性溶液被稀释,酸性减小,测得的pH偏大。(3)用来改良酸性土壤的碱是比较经济廉价、碱性稍弱的熟石灰。

 Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O
Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑