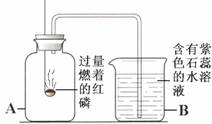
某小组在学习“二氧化碳与氢氧化钠溶液反应”时,进行了如下探究。
【提出问题】 二氧化碳与氢氧化钠反应,还是溶解在水中?
【查阅资料】 ①15 ℃、101 KPa时,二氧化碳的溶解度如下:
| 溶剂 | 水 | 酒精 |
| 溶解度 | 1.0 | 0.3 |
②15 ℃时,在酒精中氢氧化钠易溶、碳酸钠微溶。
③通常情况下,稀溶液的体积约等于溶剂的体积。
【实验设计】 在15 ℃、101 KPa时,制取二氧化碳并用于实验甲、实验乙。
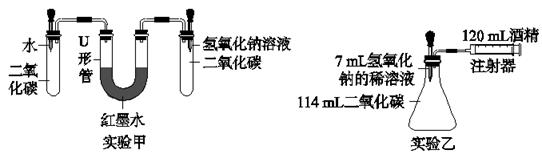
【分析与表达】 (1)如果二氧化碳与氢氧化钠反应,化学方程式是______________________,那么氢氧化钠应________保存。
(2)实验前,两套装置都进行气密性检查,实验甲装置气密性检查的方法是_____________________________________________________________________________。
(3)实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是________________________。
(4)实验乙中,将氢氧化钠完全滴入锥形瓶中,注射器会自动向内移动并将酒精推入锥形瓶,锥形瓶中能观察到的现象是____________________________________________________。
(5)实验乙中,120 mL酒精______(填“能”或“不能”)换成水,原因是_________________。
(6)实验乙结束时,注射器中酒精体积为20 mL,则与氢氧化钠反应的二氧化碳体积至少是______mL。
(7)由以上探究可知,二氧化碳能溶于水,也能与氢氧化钠反应,但实验乙的数据还不够准确,造成实验乙误差的原因可能有________________________________(写一条)。
答案
(1)2NaOH+CO2===Na2CO3+H2O 密封
(2)用热毛巾或手捂住左边的试管,U形管内液面会出现右高左低的现象,一段时间后回落到原位置,同理检验右侧试管
(3)右侧液面升高,左侧液面下降,一段时间后,右侧液面缓慢下降,左侧液面缓慢上升,最终右侧液面高于左侧液面 (4)出现白色浑浊
(5)不能 二氧化碳在水中的溶解度大于在酒精中的溶解度 (6)63
(7)水分子和酒精分子的间隔不同(或酒精具有挥发性)
解析: (2)检验装置气密性可以利用装置内外产生的压强差来验证。(3)与二氧化碳和水反应相比,二氧化碳和氢氧化钠溶液反应后,压强的变化幅度更大。(4)氢氧化钠与二氧化碳反应生成碳酸钠,碳酸钠在酒精中是微溶的,所以在锥形瓶中会出现白色浑浊。