氨水和盐酸是常见的化学试剂,可将氨气(NH3)、氯化氢气体分别溶于水制得。
![]() 工业上利用氮气和氢气反应制氨气,反应的化学方程式为______(不要求注明条件)。
工业上利用氮气和氢气反应制氨气,反应的化学方程式为______(不要求注明条件)。
![]() 小华为探究氨气溶于水是否发生化学反应,设计并完成如表实验
小华为探究氨气溶于水是否发生化学反应,设计并完成如表实验![]() 填写表中空白
填写表中空白![]() :
:
| 实验操作 | 实验现象及结论 |
| 将浸有酚酞溶液的滤纸干燥后,放入盛有干燥氨气的集气瓶中 | 无明显现象 |
| | |
(2) 小明将滴有酚酞的稀氨水加热,观察到溶液红色变浅,原因可能是______。
(4)小芳将滴有石蕊的稀盐酸加热,溶液颜色无明显变化。为进一步研究,取稀盐酸分成2份:①未经加热;②加热煮沸一段时间后冷却,分别中和等量的氢氧化钠,消耗二者的质量:①>②,则稀盐酸经加热煮沸后浓度______(填“增大![]() 、“减小”或“不变”)。
、“减小”或“不变”)。
![]() 为除去氯化钠溶液中的碳酸钠,小林设计了如图方案:
为除去氯化钠溶液中的碳酸钠,小林设计了如图方案:
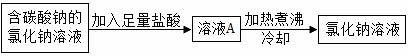
你认为上述方案______(填“合理”或“不合理”),请分析:______(如合理,说明原因;如不合理,说明原因并设计改进方案)。
答案
答案:
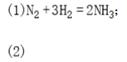 ;
;
于水是否发生化学反应,设计并完成如表实验![]() 填写表中空白
填写表中空白![]() :
:
| 实验操作 | 实验现象及结论 |
| 将浸有酚酞溶液的滤纸干燥后,放入盛有干燥氨气的集气瓶中 | 无明显现象 |
| | |
(3)氨水不稳定受热易分解生成氨气和水,导致溶液碱性减弱,则溶液颜色变浅;
(4)增大;
(5)不合理;根据上述实验,加热煮沸无法除去溶液A中混有的过量HCl;向含有碳酸钠的氯化钠溶液中边逐滴加盐酸,边测定溶液的PH至溶液呈中性即可,或将溶液加入过量的盐酸,再将溶液蒸干,然后重新配制成氯化钠溶液。
【解析】(1)氢气和氧气在一定的条件下生成氨气,反应的化学方程式为:![]() ;
;
(2)将浸有酚酞溶液的滤纸湿润后,放入盛有干燥氨气的集气瓶中,滤纸变红,说明氨气遇水溶液呈碱性;
(3)小明将滴有酚酞的稀氨水加热,观察到溶液红色变浅,原因可能是氨水不稳定受热易分解生成氨气和水,导致溶液碱性减弱,则溶液颜色变浅;
(4)取稀盐酸分成2份:①未经加热;②加热煮沸一段时间后冷却,分别中和等量的氢氧化钠,消耗二者的量:①>②,因为中和等量的氢氧化钠,未经加热的溶液用量比加热煮沸后的多,故加热煮沸后稀盐酸浓度增大;
(5)碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,所以加入稀盐酸可把碳酸钠转化为氯化钠而除去;根据上述实验,加热煮沸无法除去溶液A中混有的过量HCl;向含有碳酸钠的氯化钠溶液中边逐滴加盐酸,边测定溶液的PH至溶液呈中性即可,或将溶液加入过量的盐酸,再将溶液蒸干,然后重新配制成氯化钠溶液。故不合理。
(1)根据氮气和氢气在一定的条件下会生成氨气进行分析;
(2)氨气遇水形成氨水,溶液呈碱性,能使无色酚酞变红解答;
(3)根据氨水受热不稳定解答;
(4)根据实验现象分析解答;
(5)根据碳酸钠可与稀盐酸反应生成氯化钠、水和二氧化碳;氯化钠与稀盐酸不能发生反应解答。
本题联系学生感兴趣的实际新知识,有助于学生能力的考查,必须活学活用才能解好这类有新意的试题。解答本题关键是要知道分子在不断运动,氨水显碱性能使酚酞试液变红。