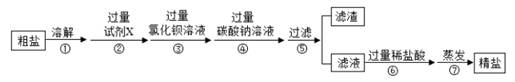
粗盐除去泥砂后含有氯化镁、硫酸钠、氯化钙等杂质,某同学对粗盐进一步提纯的实验操作过程如图所示:
(1)实验中称取5.0g粗盐,为了使粗盐充分溶解![]() 该温度下氯化钠的溶解度为36g/100g水
该温度下氯化钠的溶解度为36g/100g水![]() 量取水所用量筒的规格为______。
量取水所用量筒的规格为______。
A.10mL B.20mL C.50mL D.100mL
(2)步骤②所加试剂X的化学式为______。
(3)步骤④中加入过量碳酸钠的目的是______。
(4)步骤⑤过滤实验,制作过滤器的正确顺序为______。
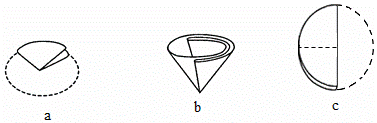
过滤后所得滤渣的化学式为______。
(5)步骤⑦蒸发实验除去______(填化学式)得到精盐。
答案
B;氢氧化钠;完全除去氯化钙和过量的氯化钡;c、a、b;![]() HCl、H2O
HCl、H2O
【解析】解:(1)设溶解5g的氯化钠至少需要水的质量x,则得:![]() ,解得:x≈13.9g 水的体积约为13.9mL,所以量取水所用量筒的规格为20mL。
,解得:x≈13.9g 水的体积约为13.9mL,所以量取水所用量筒的规格为20mL。
(2)由于氯化镁能与氢氧化钠反应生成了氢氧化镁沉淀和氯化钠,所以加入的试剂应是氢氧化钠;
(3)由于碳酸钠能与氯化钙、氯化钡反应生成了沉淀,所以步骤![]() 中加入过量碳酸钠的目的是:完全去除氯化钙和过量的氯化钡。
中加入过量碳酸钠的目的是:完全去除氯化钙和过量的氯化钡。
(4)步骤⑤过滤实验,由图示可知,制作过滤器的正确顺序为c、a、b.由于氯化镁能与氢氧化钠反应生成了氢氧化镁沉淀,氯化钡能与硫酸钠反应生成了硫酸钡沉淀,碳酸钠能与氯化钙、氯化钡反应生成了碳酸钠、碳酸钡沉淀所以,过滤后所得滤渣的化学式为:![]()
(5)由于盐酸易挥发出氯化氢气体、水受热能蒸发,所以步骤⑦蒸发实验除去HCl、H2O得到精盐。
故答为:(1)B;
(2)氢氧化钠;
(3)完全除去氯化钙和过量的氯化钡;
(4)、a、b;![]()
(5)HCl、H2O。
(1)根据氯化钠的溶解度计算、分析回答;
(2)根据氯化镁能与氢氧化钠反应生成了氢氧化镁沉淀和氯化钠分析回答;
(3)根据碳酸钠能与氯化钙、氯化钡反应分析回答;
(4)根据制作过滤器的方法和除杂质的反应分析回答;
(5)根据盐酸易挥发出氯化氢气体、水受热能蒸发分析回答。
在解此类题时,首先要知道除去的杂质的离子的性质,然后选择合适的试剂和滴加顺序进行除杂,一般加碳酸根离子要放在加钡离子之后,可以将剩余的钡离子除去,除杂的结果,最后只能剩余氯化钠,也就是氯离子和钠离子