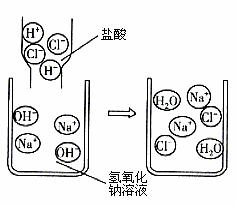
探究小组利用如图装置进行四组实验,胶头滴管盛装的是液体,烧瓶中盛装的是气体、固体或液体,当胶头滴管滴几滴液体后,能观察到气球变大的实验组合是( )
| 组合 | 滴 管 中 | 烧瓶中 |
| A | Ca(OH)2 | O2 |
| B | HCl | Zn(固) |
| C | NaOH | CO2(气) |
| D | H2SO4(浓) | H2O(液) |
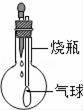

A.A B.B C.C D.D
答案
【分析】分析装置的原理:要使气球变大就要使瓶中的气体减少或瓶中温度降低。可以根据物质之间混合时的反应特点方面进行分析、判断。
【解答】解;A、氢氧化钙溶液和氧气不反应,气球不变,故A不符合题意;
B、稀盐酸和锌反应生成氢气,气球变小,故B不符合题意;
C、二氧化碳能和氢氧化钠溶液反应生成碳酸钠和水,所以气球变大,故C符合题意;
D、浓硫酸溶于水放热,所以气球会变小,故D不符合题意。
故选:C。
【点评】本题主要考查了酸、碱、盐的化学性质,解此类题的关键是分析装置的原理,再根据酸、碱、盐的性质判断物质间反应时是否有气体生成或气体参加反应。

 Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O
Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑