下列实验能达成实验目的是( )
| A | B | C | D |
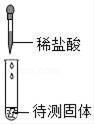
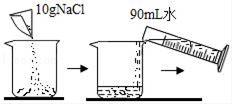
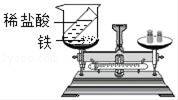
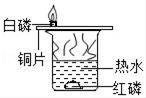
| 检验碳酸盐 | 配制质量分数10%的NaCl溶液 | 验证质量守恒定律 | 验证与氧气接触是燃烧的条件之一 |
|
|
|
|
|
A.A B.B C.C D.D
答案
【分析】A、稀盐酸能和碳酸盐、比较活泼的金属反应生成气体;
B、根据溶液质量、溶质质量分数可以计算溶质质量和水的质量;
C、铁和稀盐酸反应生成氯化亚铁和氢气;
D、红磷着火点比白磷着火点高。
【解答】解:A、实验过程中,即使产生气泡,也不能说明固体是碳酸盐,这是因为比较活泼的金属,例如铁、锌等能和稀盐酸反应生成氢气,该选项不能达到实验目的;
B、配制质量分数10%的NaCl溶液时,把10g氯化钠溶解在90mL水中恰好形成10%的氯化钠溶液,该选项能够达到实验目的;
C、铁和稀盐酸反应生成氯化亚铁和氢气,氢气逸出装置,不能用来验证质量守恒定律,该选项不能达到实验目的;
D、实验过程中,即使红磷和氧气接触,也不能燃烧,这是因为热水的温度不能达到红磷的着火点,该选项不能达到实验目的。
故选:B。
【点评】合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础。