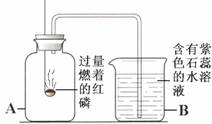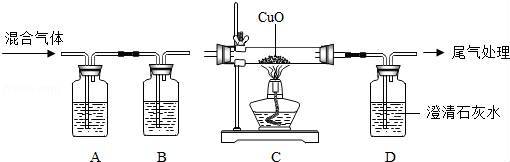

(1)A中氢氧化钠溶液的作用是 ,B中浓硫酸的作用是吸收水分,观察到C中黑色氧化铜变 ,D中澄清石灰水变浑浊,写出D中反应的化学方程式 。
(2)乙同学认为上述实验现象不能确定混合气体含有H2,他改进实验后证明了混合气体中含有H2.请写出乙同学的实验改进方法和现象 。从环境保护角度,该实验中最后导出的尾气处理方法是 。
(3)丙同学对A装置反应后的溶液成分进行验证,请根据实验现象填写下列空白处:
| 实验操作过程 | 实验现象 | 实验结论 |
| Ⅰ.取待测液少量于试管中,向其中滴加适量溶液 | 产生白色沉淀 | 溶液中含Na2CO3 |
| Ⅱ.将上述反应后的混合物静置后,再向上层清液中加入溶液。 | 溶液呈红色 | 溶液中含NaOH |
若将Ⅱ中加入的溶液换成 (写化学式),也可得出Ⅱ中相同的结论。
写出相应的化学方程式为: 。
答案
【分析】(1)根据氢氧化钠溶液能与二氧化碳反应分析作用根据一氧化碳、氢气具有还原性分析C中实验的现象,根据二氧化碳与氢氧化钙的反应写出反应的化学方程式;
(2)C中黑色氧化铜与H2反应会生产水分,改进实验后用硫酸铜粉末证明了混合气体中含有H2:无水硫酸铜变蓝色,说明有水产生;从环境保护角度,考虑该实验中最后导出的尾气处理方法;
(3)根据物质的性质可以判断鉴别物质的方法。根据实验现象和实验结论,推测加入的试剂;
【解答】解:已知“某混合气体含有CO和H2,并除去含有的少量CO2杂质”。则进行实验:
(1)因为氢氧化钠溶液与二氧化碳反应,所以A中氢氧化钠溶液的作用是除去二氧化碳,B中浓硫酸的作用是吸收水分,干燥作用;由于一氧化碳和氢气具有还原性,在加热的条件下,能将氧化铜还原为铜,所以观察到C中黑色氧化铜变变红,D中澄清石灰水变浑浊,是因为二氧化碳与氢氧化钙溶液反应产生白色沉淀,故可写出D中反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;
(2)因为“无水硫酸铜变蓝色,说明有水产生”,实验改进方法和现象在C和D之间加无水硫酸铜干燥装置,白色变蓝色,则说明有水生成。从环境保护角度(一氧化碳有毒),则该实验中最后导出的尾气处理方法是点燃或收集;
(3)对A装置反应后的溶液成分进行验证,根据实验现象和实验结论,推测加入的试剂:考虑碳酸钠与氯化钙溶液反应产生白色沉淀;考虑氢氧化钠溶液为碱性,使无色酚酞溶液变红色,故:
| 实验操作过程 | 实验现象 | 实验结论 |
| Ⅰ.取待测液少量于试管中,向其中滴加适量 CaCl2溶液 | 产生白色沉淀 | 溶液中含Na2CO3 |
| Ⅱ.将上述反应后的混合物静置后,再向上层清液中加入酚酞溶液。 | 溶液呈红色 | 溶液中含NaOH |
若将Ⅱ中加入的溶液换成CuSO4,也可得出Ⅱ中相同的结论,因为硫酸铜溶液与氢氧化钠溶液反应生成蓝色沉淀,故可写出相应的化学方程式为:2NaOH+CuSO4═Cu(OH)2↓+Na2SO4。
故答案为:
①除去二氧化碳;变红;CO2+Ca(OH)2═CaCO3↓+H2O;
②在C和D之间加无水硫酸铜干燥装置,白色变蓝色;点燃或收集。
③CuSO4. 2NaOH+CuSO4═Cu(OH)2↓+Na2SO4。
【点评】化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力。所以,对化学实验不仅要认真观察,还应掌握观察实验现象的方法。