★★★
【思路点拨】
(1)根据表中数据可知,到t5时石灰石已完全反应,共产生气体的质量为80 g-58 g=22 g;
(2)由22 g CO2根据化学方程式可求出石灰石中碳酸钙的质量,从而求出碳酸钙的质量分数;
(3)根据反应过程中数据的变化,从t0~t5时产生的气体的质量越来越多,从t5开始气体的质量不再变化。
【答案与解析】
(1)22
(2)解:设样品中含CaCO3的质量为x。
CaCO3![]() CaO+CO2↑
CaO+CO2↑
100 44
x 22 g
![]()
![]()
石灰石中CaCO3的质量分数=(50 g÷80 g)×100%=62.5%
(3)如图
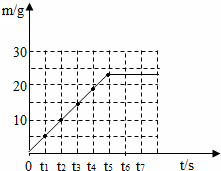
【总结升华】根据质量守恒定律可知:固体减少的质量就是生成二氧化碳的质量;由二氧化碳的质量根据碳酸钙分解的化学反应方程式就可以计算出石灰石中碳酸钙的质量分数;要想画出煅烧时生成气体的质量(m)随时间(t)变化的曲线,必须找到二者的对应关系。
答案
.某学生在课外兴趣活动中用一定量+2价金属R和稀硫酸反应来制取氢气,所做5次实验记录如下表(假设每次实验所产生的H2全部被收集,体积在同温、同压下测定,且已知在第三组实验中金属和硫酸恰好完全反应),试根据实验结果进行分析、计算,并回答下列问题:
| 实验编号 | R的质量/g | 稀硫酸的体积/mL | 生成氢气的体积/L |
| ① | 1.5 | 50 | 1.47 |
| ② | 2.0 | 50 | 1.96 |
| ③ | 2.2 | 50 | 2.16 |
| ④ | 2.5 | 50 | 2.16 |
| ⑤ | 3.0 | 50 | 2.16 |
(1)在上述实验中,金属一定过量的实验是______(填编号),稀硫酸一定过量的实验是______(填编号)。
(2)若在当时的实验条件下,H2的密度为0.085 g/L,求反应所用金属的相对原子质量是多少?
(3)若所用稀硫酸密度为1.12 g/cm。,求实验所用的稀硫酸溶液的溶质质量分数。