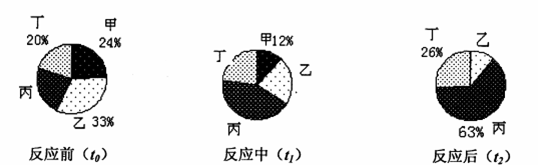
在密闭容器内进行的某反应中,测得反应前(t0)、反应中(t1)、反应后(t2)不同时刻甲、乙、丙、丁四种物质的质量分数分别如下图所示,则下列说法不正确的是( )
A. t1时刻,乙、丁、丙所占的质量分数分别为22%、23%和43% ![]() B. 若反应前甲、乙、丙、丁四种物质的总质量为100克,则再增加12克甲,甲与乙则恰好
B. 若反应前甲、乙、丙、丁四种物质的总质量为100克,则再增加12克甲,甲与乙则恰好
C. 该反应既不可能是化合反应,也不可能是分解反应 ![]() D. 若甲和丁分别是镁和碳,则该反应中甲和丁的化学计量数之比为1:2
D. 若甲和丁分别是镁和碳,则该反应中甲和丁的化学计量数之比为1:2
答案
【答案】D
【解析】【解答】A、反应前丙的质量分数是1-20%-24%-33%=23%,反应后乙的质量分数为1-26%-63%=11%,参加反应的甲、乙、丙、丁的质量比为24%:(33%-11%):(63%-23%):(26%-20%)=12:11:20:3,t1时刻,甲反应掉12%,则乙反应掉11%,丁、丙分别生成3%、20%,因此乙、丁、丙所占的质量分数分别为22%、23%和43%,A不符合题意;
B、若反应前甲、乙、丙、丁四种物质的总质量为100克,则反应前甲的质量为24g,乙33g,再增加12克甲,则反应前甲乙质量比为(24g+12g):33g=12:11,所以甲与乙则恰好完全反应,B不符合题意;
C、该反应中甲乙是反应物,丙丁是生成物,所以该反应既不可能是化合反应,也不可能是分解反应,C不符合题意;
D、若甲和丁分别是镁和碳,则该反应中甲和丁的化学计量数之比为 ![]() =2:1,D符合题意。
=2:1,D符合题意。
【分析】根据质量守恒定律分析,即化学变化中参加反应的各物质质量总和等于反应后生成的各物质的质量总和;根据化学计量数即为化学方程式中化学式前的配平系数分析。

