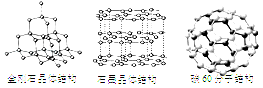
(1)金刚石、石墨、C60是由碳元素组成的三种不同单质,它们的化学性质相似,但物理性质相差很大。其原因是 。
(2)写出石墨充分燃烧的化学方程式 ;工业上可以将石墨制作成电极(石墨电极)的原因是 。
(3)木炭的主要成分与上述三种物质相同。木炭完全燃烧的产物能使紫色石蕊溶液变红,其原因是(用化学方程式进行说明) 。
答案
【分析】(1)根据金刚石、石墨、C60物理性质差异较大的原因,进行分析解答。
(2)石墨充分燃烧生成二氧化碳气体,作电极的材料应具有优良的导电性,进行分析解答。
(3)木炭完全燃烧的产物是二氧化碳,进行分析解答。
【解答】解:(1)金刚石、石墨、C60是由碳元素组成的三种不同单质,它们的化学性质相似,但物理性质相差很大,是因为碳原子的排列方式不同。
(2)石墨充分燃烧生成二氧化碳气体,反应的化学方程式为:C+O2![]() CO2。
CO2。
工业上可以将石墨制作成电极(石墨电极),是因为石墨具有优良的导电性。
(3)木炭完全燃烧的产物是二氧化碳,二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊溶液变红色,反应的化学方程式为:CO2+H2O═H2CO3。
故答案为:
(1)碳原子的排列方式不同;
(2)C+O2![]() CO2;石墨具有优良的导电性;
CO2;石墨具有优良的导电性;
(3)CO2+H2O═H2CO3。
