某同学配制50g6%氯化钠溶液,整个操作过程如下图所示,回答下列问题:
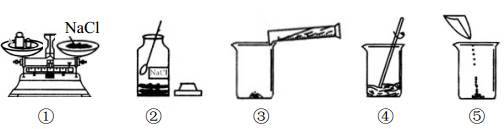
(1)配制溶液的正确操作顺序为_______(填序号,下同),其中操作错误的是________。
(2)图② 中盛放氯化钠固体的仪器名称是 ______,需称取氯化钠 _______g。
(3)量水时选用的量筒的量程最合适的是______(填序号),读数时视线要与量筒内______保持水平。
A.10 ml B.25 ml C.50ml D.100ml
(4)经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是_______(填序号)。
A.氯化钠固体不纯 B.用生锈砝码称量
C.装瓶时有少量溶液洒出 D.溶解时烧杯内壁有水珠
答案
【答案】(1)②①⑤③④ ① (2)广口瓶 3或3.0 (3)C 凹液面最低处 (4) AD
【解析】(1)配制一定溶质质量分数溶液的步骤是:计算——称量或量取——溶解——装瓶,故正确的顺序为②①⑤③④。称量时应该“左物右码”,故①操作错误。
(2)图②是盛氯化钠固体的试剂瓶,为广口瓶。配制50g6%氯化钠溶液需要称取氯化钠的质量为50g×6%=3g。
(3)50g6%氯化钠溶液需要水的质量为50g-3g=47g,体积为47ml,应选用50ml量筒,读数时视线要与量筒内凹液面最低处保持水平,不能仰视或俯视。
(4)A项,氯化钠固体不纯,称取的固体中纯净氯化钠的质量偏小,所配溶液溶质的质量分数偏小。
B项,砝码生锈后质量增加,用生锈砝码称量致使所称量的氯化钠质量增加,所配溶液溶质的质量分数偏大。
C项,溶液配制完成,质量分数不随溶液体积改变而变化,故装瓶时有少量溶液洒出,所配溶液溶质的质量分数不变。
D项,溶解时烧杯内壁有水珠,水的质量偏大,从而使溶液的质量偏大,所配溶液溶质的质量分数偏小。
故选AD。



