分析下面实验内容和结论,正确的一组是( )
| 实验内容 | 实验结论 | |
| A | 燃着的木条置于一集气瓶瓶中,木条立即熄灭 | 气体一定是CO2或N2 |
| B | 二氧化硫气体通入紫色石蕊试液中,石蕊试液变红色 | 二氧化硫具有酸性 |
| C | 用玻璃棒分别蘸取酒精和水,放在酒精灯火焰上加热片刻 | 燃烧的条件之一是物质具有可燃性 |
| D | 氯化钡溶液滴入某溶液中,出现白色沉淀 | 溶液中可能含有CO32﹣或Ag+ |
A.A B.B C.C D.D
【考点】34:化学实验方案设计与评价;4Q:常见气体的检验与除杂方法;9V:常见离子的检验方法及现象;H1:燃烧与燃烧的条件.
【分析】A、二氧化碳、氮气、稀有气体等不能燃烧,不支持燃烧;
B、二氧化硫能和水反应生成亚硫酸,亚硫酸显酸性,能使石蕊试液变红色;
C、燃烧的条件是:物质具有可燃性,有氧气参加,温度达到可燃物的着火点;
D、钡离子能和碳酸根离子结合成白色沉淀碳酸钡,氯离子能和银离子结合成白色沉淀氯化银.
【解答】解:A、二氧化碳、氮气、稀有气体等不能燃烧,不支持燃烧,燃着的木条置于一集气瓶瓶中,木条立即熄灭,气体不一定是二氧化碳或氮气,也可能是稀有气体,该选项说法不正确;
B、二氧化硫气体通入紫色石蕊试液中,石蕊试液变红色,是因为二氧化硫和水反应生成了亚硫酸,亚硫酸显酸性,能使石蕊试液变红色,不能说明二氧化硫具有酸性,该选项说法不正确;
C、酒精是可燃物,水不是可燃物,用玻璃棒分别蘸取酒精和水,放在酒精灯火焰上加热片刻,酒精燃烧起来,水不能燃烧,说明燃烧的条件之一是物质具有可燃性,该选项说法正确;
D、钡离子能和碳酸根离子结合成白色沉淀碳酸钡,氯离子能和银离子结合成白色沉淀氯化银,氯化钡溶液滴入某溶液中,出现白色沉淀,白色沉淀可能是碳酸根离子和钡离子结合成的碳酸钡,也可能是氯离子和银离子结合成的氯化银,说明溶液中可能含有CO32﹣或Ag+,该选项说法正确.
故选:CD.



| 药品 | 反应速率 |
| 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| 石灰石粉末和稀盐酸 | 产生气泡速率很快 |
| 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
登录并加入会员可无限制查看知识点解析
某化学兴趣小组利用下列装置进行O2、CO2的实验室制法和有关性质的研究。
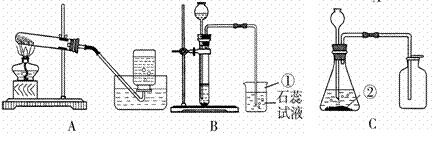 |
(1)写出下列编号仪器的名称:①_______________②______________。
(2)甲同学要用KMnO4固体来制取O2,应选用上图中的_________装置(填编号),该反应的化学方程式是_________________________________。
当O2收集满并取出集气瓶后,停止该实验的正确操作步骤是____________________
_____________________________。
(3)乙同学用浓盐酸和大理石在B装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红。对这一变化的合理解释是___________(填序号)。
A.产生的CO2直接使石蕊试液变红 B.挥发出的氯化氢溶于水使石蕊试液变红 C.产生的CO2与水反应生成H2CO3使石蕊试液变红
(4)丙同学用C装置制取了一瓶无色、无味的气体(纯净物),你推测该气体可能是___________,试用最简便的方法证实你的推测:
________________ ______________。
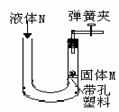
右图所示装置可用于实验室制取某些气体,并能随开随用,随关随停。下表中所选用的药品及制取的气体完全正确的一组是
选项 | 选用的药品 | 制取的气体 | |
固体M | 液体N | ||
A | 大理石 | 稀硫酸 | 二氧化碳 |
B | 锌粒 | 浓硫酸 | 氢气 |
C | 大理石 | 稀盐酸 | 二氧化碳 |
D | 碳酸钠 | 稀硫酸 | 二氧化碳 |