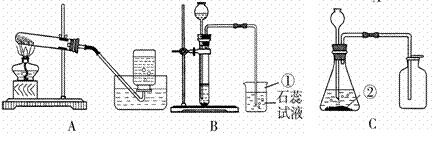
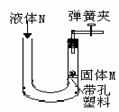
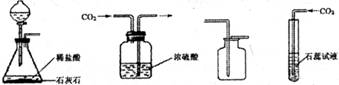
进行氧气制取与性质检验的实验.
(1)以过氧化氢溶液为原料制取并收集氧气,应选用的装置是 (选填序号).
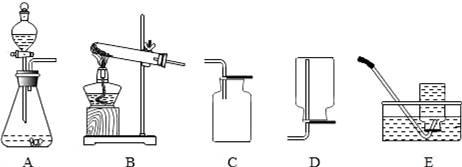

(2)实验中,用装有一定量水的集气瓶进行排水法收集氧气,能使带火星木条复燃,那么使带火星的木条复燃的氧气体积分数的最低值是多少呢?进一步展开探究.
第一组实验:5只容积均为100毫升的集气瓶,分别装入一定体积的水,再用排水法收集氧气,恰好把5只集气瓶中的水排去,将带火星的木条依次伸入5只集气瓶中,记录实验现象.
以相同方法完成第二组实验,两组实验的数据和现象见下表,(已知空气中氧气的体积分数为21%)
| 第一组 | 第二组 | |||||||||
| 集气瓶编号 | A | B | C | D | E | A | B | C | D | E |
| 集气前装入集气瓶内水的体积(毫升) | 10 | 20 | 30 | 40 | 50 | 31 | 33 | 35 | 37 | 39 |
| 带火星木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 |
①第一组实验D瓶,集气结束时氧气的体积分数为 %.
②经计算,第二组实验C瓶的氧气体积分数为48.65%,由此得出“使带火星的木条复燃的氧气体积分数的最低值只能是48.65%”的结论,对此结论和过程进行评价: .
答案
【考点】6D:氧气的制取装置;6W:探究氧气的性质.
【专题】534:常见气体的实验室制法、检验、干燥与净化;537:科学探究.
【分析】(1)根据制取气体发生装置选择的依据和收集装置的依据进行分析;
(2)分析表格可发现收集的氧气占容积的体积分数最低为35%时木条就可复燃,根据空气中原有的氧气和收集到的氧气,就可算出氧气的分数.
【解答】解:(1)以过氧化氢溶液为原料制取并收集氧气,反应物为过氧化氢,二氧化锰作催化剂,为固液反应,不需加热,故发生装置选A装置,氧气密度比空气大,不易溶于水,可以用向上排空气法,也可用排水法进行收集,但图示向上排空气法有错误,故只能选E装置,故填:AE.
(2)①集气瓶中氧气的体积分数=收集的氧气占容积的体积分数+瓶中空气占容积的体积分数×空气中氧气的体积分数,第一组实验D瓶,集气结束时氧气的体积分数为40%+60%×21%=52.6%,故填:52.6;
②该结论不严格,由图中可知,当水的体积分数达到35%时,带火星的木条复燃,水的体积分数达到33%时,带火星的木条不复燃,应作一个补充实验,当水的体积分数达到34%时,看带火星的木条是否复燃;
采取“半值法”探究能减少实验次数,实际上就是通过实验数据的分析,减少不必要的实验,第二组实验若按B、C的编号顺序进行实验,即可确定下一组实验收集的氧气占容积的体积分数应在33%~35%之间,从而省去编号A、D、E的实验,但需补充一个当水的体积分数达到34%的实验.故填:该结论不严格;实验过程可省去第二组中编号A、D、E的实验,补充一个当水的体积分数达到34%的实验.
【点评】设计实验时,要明确实验的目的,要注意控制一些变量,从而可减少实验的次数,减少实验的过程.