化学小组应用如图所示的装置进行相关实验(夹持仪器略去,K1、K2、K3均关闭,装置内所示药品的量可认为是实验中某一状态下的量),已知装置内的药品,甲:稀盐酸;乙中为无色气体;分液漏斗中为红色的溶液;丙:石灰水,依据相关信息回答问题:(碳酸钠溶液呈碱性)
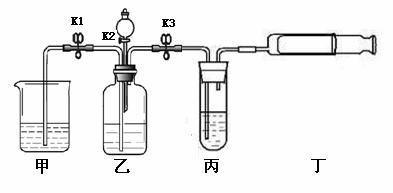
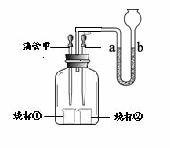

(1)打开K3,将丁向外拉,丙中长导管口有气泡冒出,且出现白色浑浊现象,则乙中的无色气体是 ,丙中出现白色浑浊的原因是 。(用化学方程式回答)(2)关闭K3,打开K2(分液漏斗上端的玻璃塞处于打开状态),当分液漏斗内的红色溶液全部进入到乙中时,关闭K2,振荡乙一会儿后,打开K1,可观察到甲中的现象是 ,乙中有气体产生,且溶液由红色变为无色,产生气体的化学方程式是 ,从物质性质的角度解释溶液由红色变为无色的原因是 。
答案
(1)CO2 Ca(OH)2 + CO2 == CaCO3↓+ H2O
(2)甲中溶液进入乙中 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 稀盐酸与碱性的溶液发生反应,使溶液失去了碱性

 2Fe + 3CO2
2Fe + 3CO2 