某兴趣小组同学对碱式碳酸铜的分解产物进行探究.
【查阅资料】
①碱式碳酸铜受热分解的化学方程式为::Cu2(OH)2CO3![]()
![]() 2CuO+H2O+CO2↑;
2CuO+H2O+CO2↑;
②白色的无水硫酸铜遇水会变成蓝色.
【实验验证】
验证碱式碳酸铜的分解产物,可选装置如图所示.
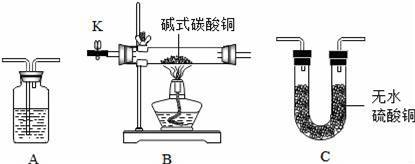

(1)如图装置A中盛放的试剂名称是 .
(2)甲同学将装置按 (填字母,且每套装置限用一次)顺序组合进行实验,验证出碱式碳酸铜的分解产物中有二氧化碳和水.
(3)B装置中粉末完全变黑后,乙同学为确认该黑色粉末是氧化铜而不是碳粉,设计如下实验,请完成下表:
| 实验步骤 | 观察到的现象 | 获得结论 | 有关反应的化学方程式 |
| 取少量黑色粉末于试管中,向其中加入足量的稀硫酸,振荡 |
| 黑色粉末均为氧化铜 |
|
【拓展探究】
丙同学利用上述实验后的B装置(包括其中药品),探究CO还原CuO所得固体产物的成分,实验装置如图: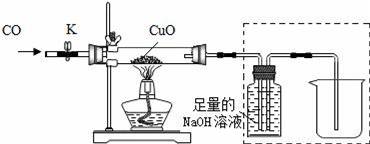

(1)实验过程
打开K,缓缓通入CO气体,一段时间后加热.当黑色固体全部变红后停止加热,继续通入CO气体直至玻璃管冷却.
(2)实验反思:上述实验装置中存在一处缺陷为:
(3)表达交流
下列有关该实验的说法正确的是 A .
A.该实验最好在通风橱中进行
B.先通入一会CO再加热是为了排净装置中的空气
C.排入到烧杯中的溶液可能显碱性,也可能显中性.
答案
【考点】实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;一氧化碳的化学性质;酸的化学性质;书写化学方程式.
【专题】科学探究.
【分析】【实验验证】(1)根据在实验室中常用澄清的石灰水来验证二氧化碳气体分析回答.
(2)根据碱式碳酸铜受热分解的生成物性质及验证的方法分析排列的顺序;
(3)根据木炭不与稀硫酸反应、氧化铜能与稀硫酸反应分析回答有关的问题;
【拓展探究】(2)根据该反应有一氧化碳生成能污染空气分析该套实验装置的明显缺陷.
(3)根据一氧化碳还原氧化铜的过程及生成物的性质分析判断有关的说法.
【解答】解:【实验验证】(1)在实验室中常用澄清的石灰水来验证二氧化碳气体,所以装置A中盛放的试剂名称是澄清石灰水.
(2)由于碱式碳酸铜受热分解生成了氧化铜、二氧化碳和水,应首先加热碱式碳酸铜,为了防止检验二氧化碳时溶液中的水对生成水的干扰,应先要验证生成的水,所以,甲同学将装置按BCA顺序组合进行实验;
(3)由于木炭不与稀硫酸反应、氧化铜能与稀硫酸反应,所以取少量黑色粉末于试管中,向其中加入足量的稀硫酸,振荡,由固体完全溶解,溶液变蓝,说明了黑色粉末均为氧化铜,反应的方程式是:CuO+H2SO4=CuSO4+H2O;
【拓展探究】
(2)由上述分析可知,该反应中生成了一氧化碳有毒能污染空气,所以,该套实验装置的明显缺陷是:没有尾气处理.
(3)A.由于尾气中含有一氧化碳有毒,该实验最好在通风橱中进行,故A正确;
B.为了防止一氧化碳与空气的混合气体点燃时发生爆炸,所以先通入一会CO再加热是为了排净装置中的空气,故B正确;
C.由装置图中虚线框内的装置的特点可知,既能吸收二氧化碳,又能收集一氧化碳,故C正确.
D.排入到烧杯中的溶液不论是碳酸钠的溶液还是碳酸钠和氢氧化钠的溶液,都显碱性.故D错误.
故答案为:
【实验验证】(1)澄清石灰水;(2)BCA;(3)固体完全溶解,溶液变蓝;CuO+H2SO4=CuSO4+H2O;
【拓展探究】(2)没有尾气处理;(3)ABC.
【点评】本题以探究的方式让学生根据实验现象和质量守恒定律来分析解答,可较好的训练学生思维,提高知识的迁移使用的能力.