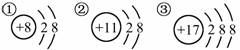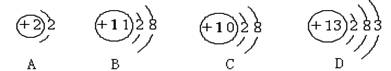下列关于Mg、Mg2+两种粒子的判断中不正确的是( )
A.核电荷数相同 B.质量几乎相等 C.Mg2+比Mg稳定 D.电子层数相同
答案
【考点】原子和离子的相互转化.
【专题】物质的微观构成与物质的宏观组成.
【分析】根据Mg2+和Mg两种粒子可以看出它们![]() 都是镁元素形成的不同微粒,据此解答.
都是镁元素形成的不同微粒,据此解答.
【解答】解:A、因它们是同种元素形成的微粒,质子数相同,故核电荷数相同,正确;
B、镁原子失去电子形成镁离子,电子的质量很小,可以忽略不计,故质量几乎相等,正确;
C、镁离子是稳定结构,镁原子易失去电子,不稳定,故镁离子比镁原子稳定,正确;
D、镁原子失去电子形成镁离子,二者的电子层数不同,错误;
故选D.
【点评】本题考查原子和离子的相互转化的知识,完成此题,可以依据已有的知识进行.

 NaCl+H2O+NH3↑
NaCl+H2O+NH3↑ NaCl+NH3↑+H2O
NaCl+NH3↑+H2O