实验室常用二氧化锰与浓盐酸来制备氯气,反应原理为:MnO2+4HCl(浓)![]()
![]() MnCl2+Cl2↑+2H2O,实验装置如图1所示.
MnCl2+Cl2↑+2H2O,实验装置如图1所示.


【查阅资料】
①氯气是黄绿色且有毒的气体,难溶于饱和食盐水;
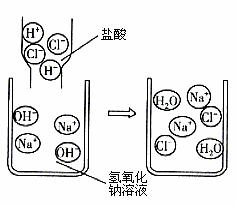
②氯气能与氢氧化钠溶液反应,生成氯化钠、次氯酸钠(NaClO)和水;
③常温常压下,氢气的密度为0.09g/L.
【回答问题】
(1)装置B的作用为 ;
(2)根据装置C判断,氯气的密度比空气 (填“大”或“小”);
(3)装置D的作 (用化学方程式表示)
【发现问题】
制备过程中,因盐酸浓度下降导致反应停止,某化学兴趣小组同学为测定装置A中反应后残余液中HCl的质量分数,提出两套测定方案如图3所示


(4)方案Ⅰ中操作m的名称为 ,通过称量生成沉淀的质量,计算出残余液中HCl的质量分数,此测定方案是 (填“可行”或“不可行”)的,原因是;
(5)方案Ⅱ利用图2装置(固定仪器的装置已略)进行测定.
①实验过程中观察到锌粒表面有气泡产生,反应的化学方程式为 ;
③当装置恢复至常温时,测得反应生成气体的体积为183.5mL,根据化学方程式计算,残余液中HCl的质量分数为多少?
【反思讨论】
(6)为了保证方案Ⅱ测定结果的准确性,正确操作是:倾斜Y形管, (填标号)
A.将残余溶液转移到锌粒中 B.将锌粒转移到残余溶液中
(7)Y形管内空气对气体体积的测量 (填“有”或“没有”)影响.
答案
【考点】常用气体的发生装置和收集装置与选取方法;常见气体的检验与除杂方法;氢气的制取和检验;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
【专题】常见气体的实验室制法、检验、干燥与净化.
【分析】(1)根据氯气、氯化氢气体、饱和食盐水的性质分析;
(2)据装置的用途分析;
(3)氯气的性质和尾气处理的方法解答;
(4)方案Ⅰ:二氧化锰与浓盐酸反应生成氯化锰,也会与硝酸银反应,故反应不可行;乙同学的方案:
(5)依据锌粒与稀盐酸反应生成氢气进行分析解答;
(6)化学反应释放热量,气体体积具有热胀冷缩的特点.
(7)氢气的密度比空气小解答.
【解答】解:(1)二氧化锰与浓盐酸来制备氯气,制取的气体中常混有挥发出的氯化氢气体,装置B的作用为除去氯化氢气体;
(2)根据装置C判断,气体长进短出,说明气体的密度比空气大;
(3)氯气有毒,排放在空气中会造成污染,故用氢氧化钠溶液吸收,反应的方程式为:Cl2+2NaOH═NaCl+NaClO+H2O;
(4)方案Ⅰ:方案Ⅰ中操作m的名称为干燥;二氧化锰与浓盐酸反应生成氯化锰,也会与硝酸银反应,故不能用来测定残余液中盐酸的质量,反应不可行;
(5)①方案Ⅱ:将锌转移到残留溶液中,反应的方程式为:Zn+2HCl=ZnCl2+H2↑;
③解:设残余液中的HCl的质量为x
Zn+2HCl=ZnCl2+H2↑
73 2
x 0.09 g/L×0.1835 L
![]()
![]() =
=![]()
![]()
X=0.6 g
残余液中HCl的质量分数:![]()
![]() ×100%=12.0%
×100%=12.0%
答:残余液中的HCl的质量分数为12.0%;
(6)将锌转移到残留溶液中,反应完毕后,每间隔1分钟读取气体体积.气体体积逐渐减小,气体体积逐渐减小的原因是气体未冷却到室温,当温度冷却到室温后,气体体积不再改变;
(7)氢气的密度比空气小,故Y形管内空气对气体体积的测量没有影响.
故答案为:(1)除去氯气中混有的氯化氢气体
(2)大
(3)Cl2+2NaOH═NaCl+NaClO+H2O
(4)干燥(或烘干) 不可行
残余液中的MnCl2也能与AgNO3溶液反应生成沉淀,造成测量值偏大
(5)①Zn+2HCl=ZnCl2+H2↑
③解:设残余液中的HCl的质量为x
Zn+2HCl=ZnCl2+H2↑
73 2
x 0.09 g/L×0.1835 L
![]()
![]() =
=![]()
![]()
X=0.6 g
残余液中HCl的质量分数:![]()
![]() ×100%=12.0%
×100%=12.0%
答:残余液中的HCl的质量分数为12.0%.
(6)B (7)没有
【点评】本题考查了对实验室制取气体的实验步骤的掌握和应用,以及依据酸的性质分析、设计实验的能力

 Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O
Na2CO3+H2O+CO2↑;然后2NH4Cl+Ca(OH)2==2NH3↑+CaCl2+H2O  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑  Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑