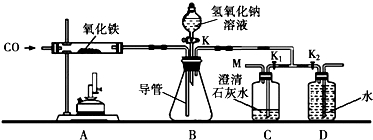
利用如图装置在实验室模拟炼铁,并将得到的尾气中的一氧化碳和二氧化碳进行分离和收集.(提示:NaOH溶液可以吸收CO2气体.)
实验步骤如下:
(1)检查装置气密性.
(2)取一定质量的氧化铁加入硬质玻璃管中,其它容器中各加入适量试剂(如图所示).
(3)关闭分液漏斗开关和K2,打开K1,通入CO气体一段时间,排除装置内的空气.此时装置存在的缺陷是 .
(4)继续通CO,在出口M处将气体干燥并用小试管收集后检验气体纯度.待装置内气体纯净后,打开分液漏斗开关K,将足量的氢氧化钠溶液放入锥形瓶中,使液面没过导管下端,关闭开关K,点燃酒精喷灯,装置A的玻璃管中反应的化学方程式是 .当装置C中的现象是 时,说明装置B中的反应是充分的,立即关闭K1,打开K2,装置D中收集到的气体是CO.
(5)一段时间后,停止加热,继续通CO气体至装置A的药品冷却.经称量氢氧化钠溶液增重2.64g,此时生成Fe的质量是 g(结果精确到0.1g).
答案
【考点】一氧化碳还原氧化铁;二氧化碳的化学性质;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
【专题】化学用语和质量守恒定律;金属与金属材料;有关化学方程式的计算.
【分析】(3)尾气中含有有毒的一氧化碳气体;
(4)根据反应原理来书写化学方程式以及氢氧化钠的性质来分析;
(5)氢氧化钠溶液增重的质量即反应中生成二氧化碳的质量,利用化学方程式进行计算.
【解答】解:(3)该装置没有尾气处理装置,故填:一氧化碳排放会造成空气污染;
(4)在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,二氧化碳进入B中,与氢氧化钠溶液反应,若C中澄清的石灰水不变浑浊则说明B中反应充分;故填:
3CO+Fe2O3![]() 2Fe+3CO2;不变浑浊;
2Fe+3CO2;不变浑浊;
(5)氢氧化钠溶液增重2.64g,即一氧化碳还原氧化铁中生成的二氧化碳的质量,设生成铁的质量为x,则
3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
112 132
x 2.64g
![]()
x≈2.2g
故填:2.2.
【点评】本题考查了根据化学方程式的计算,完成此题,可以依据题干提供的信息结合反应的化学方程式进行.

 2Fe + 3CO2
2Fe + 3CO2 