粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(Na2SO4、CaCl2、MgCl2).现以粗盐为原料制取精盐,生产过程如图所示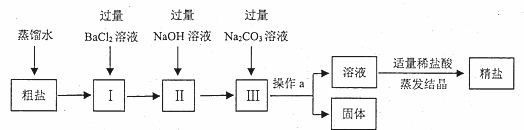
(1)写出I中发生反应的化学方程式 .加入过量BaCl2溶液的目的是 .
(2)操作a的名称是 ,该操作需要用到的玻璃仪器主要有:烧杯、 、玻璃棒.
(3)加入适量稀盐酸的作用是除去溶液中的 、 (填化学式).
(4)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是 .
答案
考点:
氯化钠与粗盐提纯;过滤的原理、方法及其应用;蒸发与蒸馏操作;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
专题:
常见的盐 化学肥料.
分析:
(1)根据氯化钡能够和硫酸钠反应产生硫酸钡沉淀和氯化钠,写出反应的方程式并分析作用;
(2)根据过滤可除去不溶性固体杂质,操作中需要漏斗等仪器;
(3)根据所加的碳酸钠和氢氧化钠均过量,分析盐酸的作用;
(4)根据蒸发操作分析玻璃棒的作用.
解答:
解:(1)氯化钡能够和硫酸钠反应产生硫酸钡沉淀和氯化钠,其中过量的氯化钡可以将硫酸钠杂质完全除去;故答案为:Na2SO4+BaCl2═BaSO4↓+2NaCl;使硫酸钠杂质完全除去;
(2)经过操作a得到固体和液体,因此是过滤操作,过滤中还需要的玻璃仪器是漏斗;故答案为:过滤;漏斗;
(3)由于加入的碳酸钠和氢氧化钠都是过量的,所以加入盐酸是为的与过量的碳酸钠和氢氧化钠反应,故答案为:NaOH、Na2CO3;
(4)蒸发时,要使用玻璃棒不断的搅拌,防止受热不均,使液滴飞溅;故答案为:防止受热不均,使液滴飞溅.
点评:
本题考查了粗盐提纯的相关问题,很好的考查了学生根据所学知识分析和解决问题的能力,尤其是除杂知识的应用.