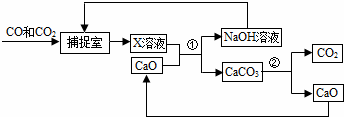
工业上常用“碳捕捉”技术将CO和CO2混合气体中的CO2捕捉并回收CO,其基本过程如图所示(部分条件及物质未标出).
(1)反应②分离出的CO2可制成干冰,干冰常用于
(2)反应①在“反应分离室”内进行.将NaOH溶液与CaCO3分离的操作是
需要用到的玻璃仪器有
(3)“捕捉室”中发生反应的化学方程式为
(4)下列有关该捕捉过程的叙述正确的有( )
A.捕捉到的CO2可制备其它化工产品,减少了温室气体排放.
B.回收的CO可直接排放到大气中.
C.整个过程中,只有一种物质可循环利用.
D.能耗大是该捕捉技术的一大缺点.
答案
(1)制冷剂(或人工降雨)
(2)过滤 烧杯、漏斗、玻璃棒
(3)CO2 + 2NaOH = NaCO3 + H2O (2分) (4) A D

 2Fe + 3CO2
2Fe + 3CO2 