|
教案示例 |
|
|
课题 3 溶质的质量分数
教学目标
1 . 掌握一种溶液组成的表示方法——溶质的质量分数,能进行溶质质量分数的简单计算。
2 . 初步学会配制一定溶质质量分数的溶液。
教学重点:溶液的溶质质量分数的概念和简单的计算以及配制一定溶质质量分数的溶液。
教学难点:溶液的质量分数的概念的引入。
教学过程
一、引入新课
在实际应用中,常要准确知道一定量的溶液里含有溶质的质量。如在施用农药时,过浓会毒害农作物,过稀则不能有效地杀虫灭菌。因此,我们需要知道溶液的浓稀程度,也就是溶液的组成。
二、新课学习
1 . 溶质的质量分数
演示 9-5
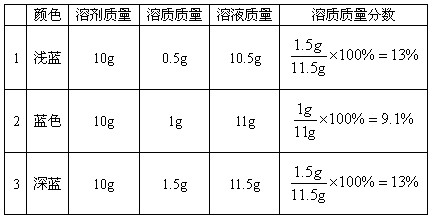
在 3 支试管中各加入 10mL 的水,然后分别加入约 0.5g 、 1g 、 1.5g 的固体硫酸铜,然后观察现象。
1 2 3

颜色: 浅蓝 蓝色 深蓝
判断依据:一定量溶液里,所含溶质的多少。
思考:溶液的浓稀和溶液的饱和与否的关系。同一温度时,同一溶质的饱和溶液肯定比不饱和溶液浓。
从硫酸铜溶液的颜色我们可以判别除这 3 个试管中,溶液的浓稀程度是不一样的,颜色越深,说明这个溶液越浓。但是如果这个溶液是无色透明的,我们要怎样辨别一个溶液的浓稀程度呢?或者说需要知道确切的某一溶液中含有溶质的质量的时候,要怎么办?
接下来我们就来了解一种表示溶液组成的方法:溶质的质量分数。溶液中溶质的质量分数是溶质的质量与溶液的质量之比:
![]()
接下来我们来计算刚才 3 种硫酸铜溶液中溶质硫酸铜的质量分数。
演示 9-6 :
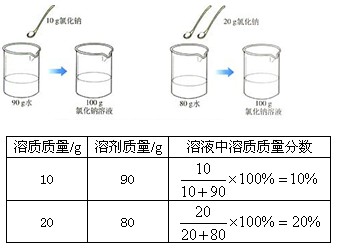
2 .计算
例题 1. 在农业生产中,常需要用质量分数为 16% 的氯化钠溶液来选种。现要配制 150kg 这种溶液,需要氯化钠和水的质量各是多少?

答:配 150kg 质量分数为 16% 的氯化钠溶液需要 24kg 氯化钠和 126kg 水。
例题 2 . 化学实验室现在有 98% 的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把 50g 质量分数为 98% 的浓硫酸稀释为质量分数为 20% 的硫酸溶液,需要多少克水?
分析:解决这道题的关键就是知道溶液稀释前后溶质的质量不变,也就是
![]() ,这道题我们可以用未知数来求解。
,这道题我们可以用未知数来求解。
设:稀释后溶液的质量为
![]() 。
。
![]()
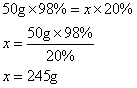
需要水的质量 =245g-50g=195g
答:把 50g 质量分数为 98% 的浓硫酸稀释成为质量分数为 20% 的硫酸溶液,需要 195g 水。
想一想,如果把 50g 换成 50mL ,还需要什么条件?
3 .配置溶质质量分数一定的溶液
配置步骤:
(1) 计算:需食盐: 150g × 16%=24g 需水: 150g–24g=126g 。
(2) 称量:用天平称量 24g 食盐 用量筒量取 126mL 水。
(3) 溶解:烧杯、玻璃棒。
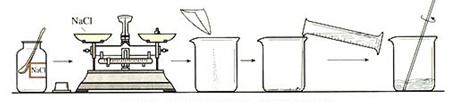
实验仪器:天平(砝码)、药匙、量筒、胶头滴管、烧杯、玻璃棒。
三、小结
在溶液中溶质的质量分数就是溶质质量与溶液质量之比,我们也可以根据这个关系配制溶质质量分数一定的溶液。
四、板书设计
