推理是学习化学的一种重要方法,下列推理合理的是( )
A.离子是带电荷的粒子,则带电荷的粒子一定是离子
B.单质是由同种元素组成的,则只含一种元素的纯净物一定是单质
C.中和反应有盐和水生成,则有盐和水生成的反应一定是中和反应
D.溶液具有均一性和稳定性,则具有均一性和稳定性的液体一定是溶液
B
【解析】
A、离子是带电荷的微粒,但带电荷的微粒不一定是离子,也可能是质子、电子等,错误;B、单质是由同种元素组成的纯净物,则只含一种元素的纯净物一定是单质,正确;
C、中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如CO2+2NaOH═Na2CO3+H2O,错误;D、溶液具有均一性和稳定性,但具有均一性和稳定性的液体不一定是溶液如水,错误。故选B。
点睛:中和反应是酸与碱作用生成盐和水的反应。反应物是酸和碱,生成物是盐和水,两者缺一不可。
下列有关溶液的叙述错误的是( )
A.长期放置后不会分层的液体一定是溶液
B.衣服上的油污用汽油或用加了洗涤剂的水可除去
C.一瓶合格的生理盐水密封一段时间,不会出现浑浊
D.实验室常将固体药品配制成溶液进行化学反应,以提高反应速率
A
【详解】
A、溶液是均一稳定的混合物,长期放置后不会分层的液体不一定是混合物,例如蒸馏水,正确;B、汽油能溶解油污,洗涤剂对油污有乳化作用,错误;C、溶液具有稳定性,密封一段时间,不会出现浑浊,错误;D、溶液中进行的反应接触面积大,反应速率快,错误。故选A。
【点睛】
溶液是均一、稳定的混合物。
向一定质量的水中加入生石灰,下列曲线错误的是
A.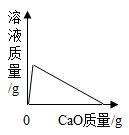 B.
B.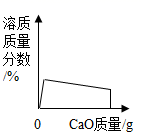 C.
C.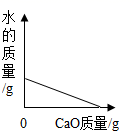 D.
D.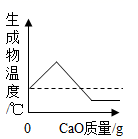
D
【解析】
A、氧化钙与水反应生成氢氧化钙,溶液质量增加。当溶液饱和后溶液质量最大,继续加入氧化钙,氧化钙与水继续反应,当水反应完后,溶液质量为0,正确;B、氧化钙与水反应生成氢氧化钙,溶质质量分数增大。当溶液饱和后,溶质质量分数最大;继续加入氧化钙,氧化钙与水继续反应,溶液温度升高,氢氧化钙溶解度变小,溶质质量分数减小,当水反应完后,溶液质量分数为0,正确;C、氧化钙与水反应生成氢氧化钙,当加入氧化钙达到一定量时恰好与水完全反应,此时水的质量为0,正确;D、氧化钙与水反应温度升高,当氧化钙恰好与水完全反应后温度最高,此后温度开始降低,但不会低于反应前的温度,错误。故选D。
点睛:要准确解答此类题,关键要对化学反应的知识熟练掌握,并能结合图象的数学意义,综合考虑;图象的意义要抓住三点:①抓图象的起点,②抓图象的终点,③抓图象的变化过程。
除去下列物质中混有的少量杂质,实验操作正确的是( )
| 选项 | 物质 | 杂质 | 实验操作 |
| A | CaO | CaCO3 | 加稀盐酸至不再有气泡产生,过滤 |
| B | KCl | MnO2 | 加足量水溶解,过滤,蒸发 |
| C | O2 | CO | 通过灼热的铜网 |
| D | Na2SO4溶液 | H2SO4 | 加入过量BaCl2溶液,过滤 |
A.A B.B C.C D.D
B
【分析】
根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变。除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
【详解】
A、CaO和CaCO3均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误;
B、KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法正确;
C、一氧化碳与氧气的混合气体再通过灼热的铜网时可能会发生爆炸,不符合除杂原则,故选项所采取的方法错误;
D、Na2SO4溶液、H2SO4均能与过量BaCl2溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误。故选B。
【点睛】
物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键。
下列物质不属于溶液的是( )
A.碘酒 B.矿泉水 C.白醋 D.蒸馏水
D
【解析】
A、碘酒是碘的酒精溶液,符合溶液的定义,是溶液,故错误;
B、矿泉水中含有矿物质,是溶液,故错误;
C、白醋是醋酸的水溶液,是溶液,错误;
D、蒸馏水是一种物质,是纯净物,不是混合物,故不属于溶液,故正确
【点睛】
溶液是具有均一性和稳定性的混合物;
本卷还有95题,登录并加入会员即可免费使用哦~

该作品由: 用户123456分享上传
可圈可点是一个信息分享及获取的平台。不确保部分用户上传资料的来源及知识产权归属。如您发现相关资料侵犯您的合法权益,请联系 可圈可点 ,我们核实后将及时进行处理。